题目内容
【题目】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是。
(2)该反应中,发生还原反应的过程是→。
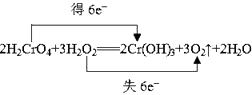
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目:。
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为L。
【答案】
(1)H2O2
(2)H2CrO4,Cr(OH)3
(3)
(4)3.36
【解析】(1)H2O2生成氧气,化合价从1升高到0,被氧化,作为还原剂;
(2)发生还原反应的过程是化合价降低的过程,分析五种物质中,只有H2CrO4的Cr元素化合价降低,生成Cr(OH)3;
(4)由双氧水生成氧气,每生成1 mol氧气,转移2 mol电子,故转移0.3 mol电子,能生成0.15 mol氧气,故体积为0.15 mol×22.4 L/mol=3.36 L。

练习册系列答案
相关题目