题目内容
下列表达方式错误的是( )
A、溴化钠的电子式: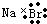 | ||
B、S2-的结构示意图: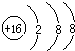 | ||
C、O-18的原子符号:
| ||
| D、CO2分子的结构式:O=C=O |
分析:A.溴化钠为离子化合物,钠离子和溴离子表示都错误;
B.硫离子核电荷数为16,核外电子数为18;
C.O-18的原子的质子数为8,质量数为18;
D.二氧化碳为直线型结构,分子中存在两个碳碳双键.
B.硫离子核电荷数为16,核外电子数为18;
C.O-18的原子的质子数为8,质量数为18;
D.二氧化碳为直线型结构,分子中存在两个碳碳双键.
解答:解:A.溴化钠中存在钠离子和溴离子,电子式中必须标出所带电荷,溴化钠的电子式为: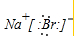 ,故A错误;
,故A错误;
B.S2-的核电荷数为16,核外电子总数是18,硫离子的结构示意图为: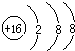 ,故B正确;
,故B正确;
C.18O的质子数为8,该氧原子的表示为:
O,故C正确;
D.CO2分子中存在两个碳氧双键,为直线型结构,二氧化碳的结构式为:O=C=O,故D正确;
故选A.
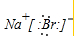 ,故A错误;
,故A错误;B.S2-的核电荷数为16,核外电子总数是18,硫离子的结构示意图为:
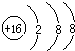 ,故B正确;
,故B正确;C.18O的质子数为8,该氧原子的表示为:
18 8 |
D.CO2分子中存在两个碳氧双键,为直线型结构,二氧化碳的结构式为:O=C=O,故D正确;
故选A.
点评:本题考查了电子式、离子结构示意图、结构式的表示方法,题目难度中等,注意明确结构式、电子式与分子式的概念、表示方法及其区别,明确离子化合物与共价化合物电子式的表示方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列表达方式错误的是( )
A、二氧化碳的电子式是 | ||
B、氟化钠的电子式 | ||
C、S2-离子的结构示意图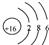 | ||
D、镁-24原子
|
下列表达方式错误的是( )
A、甲烷的电子式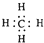 | ||
B、氟化钠的电子式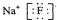 | ||
C、硫离子的结构示意图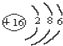 | ||
D、碳-12原子
|