题目内容
12.合金是重要的金属材料.请回答下列问题:(1)下列物品所使用的主要材料属于合金的是C(填字母)
A.青花瓷瓶 B.橡胶充气艇 C.不锈钢锅
(2)生铁是常用的合金,生铁属于混合物(填“纯净物”和“混合物”).
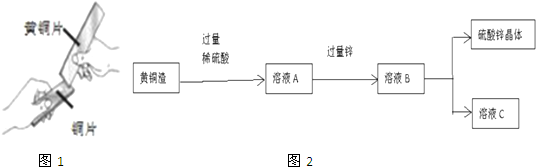
(3)黄铜是铜锌合金,将纯铜片和黄铜片互相刻画(如图所示),纯铜片上留下了明显的划痕,这说明黄铜的硬度比纯铜的硬度大
(4)黄铜渣中约含Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质.处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):
①溶液A 中主要含ZnSO4、CuSO4 和H2SO4,则Ⅱ中反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑、Zn+CuSO4=ZnSO4+Cu
②下列说法不正确的是d(填字母)
a.Ⅰ和Ⅱ中的操作均包含过滤
b.溶液A 中ZnSO4 的质量大于CuSO4
c.溶液A 的质量小于溶液B
d.溶液C 中溶液的质量分数小于溶液B
分析 (1)合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质;
(2)合金属于混合物;
(3)合金要比组成它的纯金属的硬度大;
(4)根据金属与酸、盐的溶液反应的规律书写化学方程式.
解答 解:(1)青花瓷瓶属于硅酸盐材料;橡胶充气艇属于有机高分子材料;不锈钢锅属于合金;
故答案为:C;
(2)生铁是常用的合金,合金属于混合物,故生铁属于混合物;
故答案为:混合物;
(3)将纯铜片和黄铜片互相刻画,纯铜片上留下明显的划痕,说明黄铜的硬度比纯铜的硬度大;
故答案为:黄铜的硬度比纯铜的硬度大;
(4)①由于锌排在氢和铜的前面,故锌既可以与酸反应,也可以与硫酸铜反应,反应的化学方程式分别为:Zn+H2SO4═ZnSO4+H2↑,Zn+CuSO4=ZnSO4+Cu,
故答案为:Zn+H2SO4═ZnSO4+H2↑;Zn+CuSO4=ZnSO4+Cu;
②a.由图可知,操作Ⅰ过滤除去铜和杂质,操作Ⅱ过滤是除去锌和置换出的铜,故a正确;
b.因氧化锌的质量大于氧化铜,另外锌也能和硫酸反应生成硫酸锌,而铜和硫酸不反应,故溶液A中硫酸锌的质量大于硫酸铜,故b正确;
c.溶液A加入锌后,反应的化学方程式分别为:Zn+H2SO4═ZnSO4+H2↑,Zn+CuSO4=ZnSO4+Cu;对反应Zn+H2SO4═ZnSO4+H2↑分析可知,每65份质量的锌进入溶液,从溶液中出来2份质量的氢气,使得溶液质量增加,对于反应Zn+CuSO4=ZnSO4+Cu来说,每65份质量的锌进入溶液,从溶液中析出64份质量的铜,也使得溶液质量增大,故溶液A的质量小于溶液B,故c正确;
d.溶液C为饱和溶液,质量分数达到同温度下的最大值,故d错误,
故答案为:d.
点评 本题考查合金以及物质分离和提纯的方法,题目难度中等,注意制备原理的掌握是解题的关键.

 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案| A. | CO2 | B. | H2O | C. | NaOH | D. | BaCl2 |
| A. | 0.2 mol•L-1盐酸与等体积0.05 mol•L-1Ba(OH)2溶液混合后,溶液pH为1 | |
| B. | 0.1mol•L-1CH3COOH溶液加水稀释,n(H+)增大 | |
| C. | 向NH4Cl溶液中逐渐加入适量NaOH固体,溶液的导电性明显增强 | |
| D. | 等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液显酸性:c(HX)>c(Na+)>c(X-) |
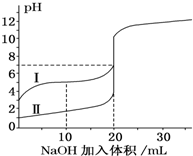 室温下,用0.100mol/L NaOH 溶液分别滴定20.00mL 0.100mol/L的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
室温下,用0.100mol/L NaOH 溶液分别滴定20.00mL 0.100mol/L的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )| A. | V(NaOH)=10.00 mL 时,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$>1 | |
| B. | Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线 | |
| C. | pH=7时,两种酸所用NaOH溶液的体积相等 | |
| D. | V(NaOH)=20.00 mL 时,c(Cl-)<c(CH3COO-) |
| A. | 味觉上具有酸味的食物就是酸性食物 | |
| B. | Fe3O4俗称铁红,常做红色油漆和涂料 | |
| C. | 氢氧化铝、氢氧化钠、碳酸钠都是常见的胃酸中和剂 | |
| D. | “地沟油”禁止食用,但处理后可用来制肥皂和生物柴油 |
| A. | 水 | B. | CCl4 | C. | 氨水 | D. | 水银 |
| A. | 伴有能量变化的物质变化都是化学变化 | |
| B. | 没有物质的变化,就没有能量的变化 | |
| C. | 热化学方程式中,化学式前面的化学计量数只表示物质的量,不表示微粒数 | |
| D. | 热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据 |
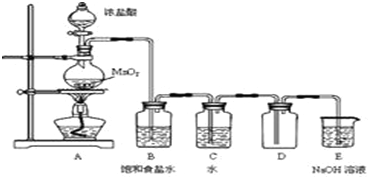
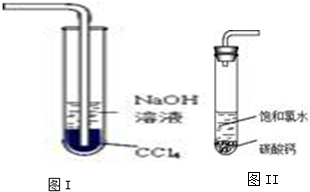
 2013年12月15日4时搭载长征系列火箭的“玉兔号”顺利驶抵月球表面,实现了五星红旗耀月球的创举.火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4做氧化剂.请回答下列问题:
2013年12月15日4时搭载长征系列火箭的“玉兔号”顺利驶抵月球表面,实现了五星红旗耀月球的创举.火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4做氧化剂.请回答下列问题: