题目内容
【题目】肼(N2H4)是一种无色易溶于水的油状液体。具有碱性和极强的还原性,在工业生产中应用非常广泛。
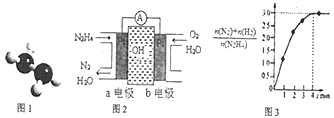
(1)已知肼的球棍棋型如图1所示,试写出肼的电子式:________。
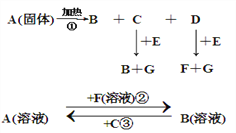
(2)目前正在研发的一种肼燃料电池的结构如图2所示。________(填“a”或“b”)电极为电池的负极。
(3)在1L固定体积的容器中加入0.1molN2H4,在303K、Pt催化下发生:N2H4(I)![]() N2(g)+2H2(g),测得容器中
N2(g)+2H2(g),测得容器中![]() 与时间关系如图3所示,则04min氮气的平均速率v(N2)=________。
与时间关系如图3所示,则04min氮气的平均速率v(N2)=________。
【答案】 ![]() a 0.0125mol·L-1·min -1
a 0.0125mol·L-1·min -1
【解析】(1)根据肼的球棍棋型可知肼的电子式为![]() 。(2)肼失去电子,在负极通入,氧气得到电子,在正极通入,因此a电极为电池的负极。(3)根据方程式可知
。(2)肼失去电子,在负极通入,氧气得到电子,在正极通入,因此a电极为电池的负极。(3)根据方程式可知
N2H4(l)![]() N2(g)+2H2(g)
N2(g)+2H2(g)
起始量(mol) 0.1 0 0
转化量(mol) x x 2x
4min时(mol) 0.1-x x 2x
根据图像可知![]() ,解得x=0.05,所以04min氮气的平均速率v(N2)=
,解得x=0.05,所以04min氮气的平均速率v(N2)= ![]() =0.0125mol·L-1·min -1 。
=0.0125mol·L-1·min -1 。

练习册系列答案
相关题目