题目内容
Q、R、X、Y、Z是原子序数依次增大的五种短周期元素,在短周期的所有元素中Q的原子半径与Z的原子半径之比最小(不包括稀有气体),R、X、Y三种元素的原子核外电子层数相同,同一周期中R的一种单质的熔点最高,Y与Q、R、X、Z均能形成多种常见化合物.(1)X在周期表中的位置:______,其原子核外有______种不同形状的电子云.这五种元素中,最外层有两个未成对电子的元素是______(用元素符号表示).
(2)ZYQ的电子式是______.
(3)Q分别与X.Y形成的最简单化合物的稳定性______>______(用分子式表示)
(4)Q与R两元素组成的分子构型可能是______(填写序号).
a.直线型 b.平面形 c.三角锥形 d.正四面体
(5)常温下液态化合物甲只含上述元素中的两种,分子中原子个数比1:1,请你仅用一个化学方程式表示甲既有氧化性又有还原性______ 2H2O+O2↑
【答案】分析:Q、R、X、Y、Z是原子序数依次增大的五种短周期元素,在短周期的所有元素中Q的原子半径与Z的原子半径之比最小,则Q的原子半径最小,应为H元素,Z的原子半径最大,应为Na元素,R、X、Y三种元素的原子核外电子层数相同,应为同一周期元素,为第而周期元素,第二周期中R的一种单质的熔点最高,则R为C元素,熔点最高的单质为金刚石,Y与Q、R、X、Z均能形成多种常见化合物,则Y为O元素,与其它物质反应形成多种氧化物,根据Q、R、X、Y、Z是原子序数依次增大的五种短周期元素,可知X为N元素,以此解答题中各小问.
解答:解:Q、R、X、Y、Z是原子序数依次增大的五种短周期元素,在短周期的所有元素中Q的原子半径与Z的原子半径之比最小,则Q的原子半径最小,应为H元素,Z的原子半径最大,应为
Na元素,R、X、Y三种元素的原子核外电子层数相同,应为同一周期元素,为第而周期元素,第二周期中R的一种单质的熔点最高,则R为C元素,熔点最高的单质为金刚石,Y与Q、R、X、Z均能形成多种常见化合物,则Y为O元素,与其它物质反应形成多种氧化物,根据Q、R、X、Y、Z是原子序数依次增大的五种短周期元素,可知X为N元素,
(1)X为N元素,位于第二周期第VA族,核外电子排布为1S22S22P3,有S和P两种不同形状的电子云,最外层有两个未成对电子,则最外层的电子排布可能为nP2或nP4,只有C、O两种元素符合,
故答案为:第二周期第VA族;2;C、O;
(2)ZYQ组成的化合物为NaOH,为离子化合物,其电离子式为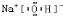 ,故答案为:
,故答案为: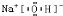 ;
;
(3)Q分别与X、Y形成的最简单化合物分别为NH3和H2O,元素的非金属性越强,则对应的氢化物的稳定性越强,O元素的非金属性大于N元素的非金属性,则有H2O>NH3,
故答案为:H2O>NH3;
(4)Q与R两元素组成的分子为烃类物质,其中甲烷为正四面体结构,乙烯为平面结构,乙炔为直线形结构,
故答案为:abd;
(5)常温下液态化合物有H2O2和H2O,H2O2分子中原子个数比1:1,在二氧化锰做催化剂条件下发生分解反应生成氧气和水,反应的方程式为2H2O2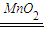 2H2O+O2↑,
2H2O+O2↑,
故答案为:2H2O2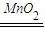 2H2O+O2↑.
2H2O+O2↑.
点评:本题考查原子结构与元素周期律的关系,题目难度不大,正确推断元素的种类是解答本题的关键,要正确把握元素周期律的递变规律.
解答:解:Q、R、X、Y、Z是原子序数依次增大的五种短周期元素,在短周期的所有元素中Q的原子半径与Z的原子半径之比最小,则Q的原子半径最小,应为H元素,Z的原子半径最大,应为
Na元素,R、X、Y三种元素的原子核外电子层数相同,应为同一周期元素,为第而周期元素,第二周期中R的一种单质的熔点最高,则R为C元素,熔点最高的单质为金刚石,Y与Q、R、X、Z均能形成多种常见化合物,则Y为O元素,与其它物质反应形成多种氧化物,根据Q、R、X、Y、Z是原子序数依次增大的五种短周期元素,可知X为N元素,
(1)X为N元素,位于第二周期第VA族,核外电子排布为1S22S22P3,有S和P两种不同形状的电子云,最外层有两个未成对电子,则最外层的电子排布可能为nP2或nP4,只有C、O两种元素符合,
故答案为:第二周期第VA族;2;C、O;
(2)ZYQ组成的化合物为NaOH,为离子化合物,其电离子式为
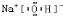 ,故答案为:
,故答案为: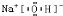 ;
;(3)Q分别与X、Y形成的最简单化合物分别为NH3和H2O,元素的非金属性越强,则对应的氢化物的稳定性越强,O元素的非金属性大于N元素的非金属性,则有H2O>NH3,
故答案为:H2O>NH3;
(4)Q与R两元素组成的分子为烃类物质,其中甲烷为正四面体结构,乙烯为平面结构,乙炔为直线形结构,
故答案为:abd;
(5)常温下液态化合物有H2O2和H2O,H2O2分子中原子个数比1:1,在二氧化锰做催化剂条件下发生分解反应生成氧气和水,反应的方程式为2H2O2
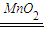 2H2O+O2↑,
2H2O+O2↑,故答案为:2H2O2
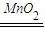 2H2O+O2↑.
2H2O+O2↑.点评:本题考查原子结构与元素周期律的关系,题目难度不大,正确推断元素的种类是解答本题的关键,要正确把握元素周期律的递变规律.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目