题目内容
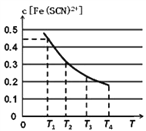
【题目】短周期元素W,X,Y,Z在元素周期表中的位置如图所示.下列说法中,正确的是( ) 
A.W的最高价氧化物对应的水化物是强酸
B.Y的原子半径在同周期主族元素中最大
C.W的非金属性比Z的弱
D.Z的气态氢化物的稳定性在同主族元素中最强
【答案】A
【解析】解:由元素所在周期表中的位置可知X为He,Y为F,W为Cl,Z为S,则A.W为Cl,非金属性较强,对应的最高价氧化物对应的水化物为HClO4 , 为酸性最强的含氧酸,故A正确;
B.同周期元素从左到右原子半径逐渐减小,则Y的原子半径在同周期主族元素中最小,故B错误;
C.同周期元素从左到右,元素的非金属性逐渐增强,则W的非金属性比Z的强,故C错误;
D.同主族元素从上到下,元素的非金属性逐渐增强,对应的元素的非金属性越强,对应的氢化物越稳定,W为S,同主族元素中O对应的氢化物的稳定性最强,故D错误.
故选A.

【题目】H2O2是一种绿色氧化还原试剂,在化学研究中应用广泛.
(1)某小组拟在同浓度Fe3+的催化下,探究H2O2浓度对H2O2分解反应速率的影响.限选试剂与仪器:30% H2O2、0.1molL﹣1 Fe2(SO4)3、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器①写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:
②设计实验方案:在不同H2O2浓度下,测定(要求所测得的数据能直接体现反应速率大小).
③设计实验装置,完成如1图所示的装置示意图.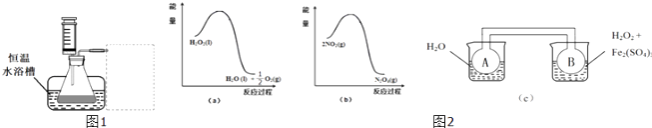
④参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据;数据用字母表示).
实验序号 | V[0.1molL﹣1 Fe2(SO4)3]/mL | ||||
1 | a | ||||
2 | a |
(2)利用图2(a)和2(b)中的信息,按图2(c)装置(连能的A、B瓶中已充有NO2气体)进行实验.可观察到B瓶中气体颜色比A瓶中的(填“深”或“浅”),其原因是 .