题目内容
15.把ag Na0H样品(杂质不与硫酸反应)加入到含bmol H2SO4的溶液中,充分反应后,为中和多余的酸,用去c g KOH,求样品中Na0H的质量分数.分析 根据题意,加入bmol H2SO4和cgKOH,最终溶液刚好成中性,则根据氢离子等于氢氧根列方程求解.
解答 解:根据题意,加入bmol H2SO4和cgKOH,最终溶液刚好成中性,所以氢离子、氢氧根离子的物质的量相等,设样品中Na0H的物质的量为xmol,则有x+$\frac{c}{56}$=b×2,解得x=2b-$\frac{c}{56}$,所以样品中Na0H的质量分数为:$\frac{(2b-\frac{c}{56})×40}{a}$×100%=$\frac{560b-5c}{7a}$×100%,答:样品中Na0H的质量分数为$\frac{560b-5c}{7a}$×100%.
点评 本题考查学生利用方程式的简单计算,关键明确溶液刚好成中性,根据氢离子等于氢氧根列方程是解题关键.

练习册系列答案
相关题目
6.下列说法不正确的是( )
| A. | 硫酸的摩尔质量(g/mo1)与6.02×1023个磷酸分子的质量(g)在数值上相等 | |
| B. | 6.02×1023个N2和6.02×1023个O2的质量比等于7:8 | |
| C. | 3.2gO2所含的原子数目约为0.2×6.02×1023个 | |
| D. | 常温、常压下,0.5×6.02×1023个二氧化碳分子的质量是44g |
20.己知甲烷和氧气的混合气中,甲烷的质量分数为20%,则甲烷和氧气的物质的量之比为( )
| A. | 1:4 | B. | 1:5 | C. | 1:4.5 | D. | 1:2 |
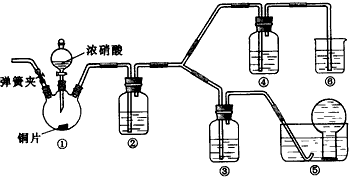
5.下列各组物质的分离可用分液漏斗的是( )
| A. | 乙醇和水 | B. | 香油和食盐水 | ||
| C. | 黄河水中的泥沙与水 | D. | 食盐水中获得食盐 |
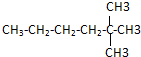 用“键线式”可表示为
用“键线式”可表示为 ,其中每个端点和转折点都表示一个碳原子,氢原子已省略.某有机物分子用键线式表示为
,其中每个端点和转折点都表示一个碳原子,氢原子已省略.某有机物分子用键线式表示为 ,该有机物的分子式为:C10H20,其一氯代物有4种.
,该有机物的分子式为:C10H20,其一氯代物有4种.