题目内容
(1)1molO2与足量氢气反应产生水蒸气放热483.6kJ,若1g水蒸气转化成液态水放热2.444kJ,请写出表示氢气燃烧热的热化学方程式:______.
(2)由汽油裂解得到乙烯、丙烯是重要的化工原料,请写出下列转化的方程式,并注明反应类型.
丙烯→聚丙烯______
(3)将N2、H2置于容积为2L的密闭容器中,发生反应,反应进行到4S末,测得N22mol、H21.5mol、NH32mol.则用氮气浓度的减少来表示该反应速率为______.
(4)在500ml密闭容器中,将2molA和1molB混合加热到500℃,达到平衡2A(g)+B(g)?3C(g)K=16求A转化为C的转化率为______.
(5)在密闭容器中发生下列反应:aA(g)?cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,A的浓度为原平衡的2.1倍,则a______c+d(填“>”、“=”或“<”).
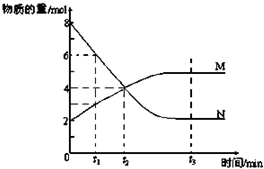
(6)在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,反应的化学方程式为______.
(2)由汽油裂解得到乙烯、丙烯是重要的化工原料,请写出下列转化的方程式,并注明反应类型.
丙烯→聚丙烯______
(3)将N2、H2置于容积为2L的密闭容器中,发生反应,反应进行到4S末,测得N22mol、H21.5mol、NH32mol.则用氮气浓度的减少来表示该反应速率为______.
(4)在500ml密闭容器中,将2molA和1molB混合加热到500℃,达到平衡2A(g)+B(g)?3C(g)K=16求A转化为C的转化率为______.
(5)在密闭容器中发生下列反应:aA(g)?cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,A的浓度为原平衡的2.1倍,则a______c+d(填“>”、“=”或“<”).
(6)在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,反应的化学方程式为______.

(1)1mol O2与足量氢气反应产生水蒸气放热483.6kJ,反应的热化学方程式为:①H2(g)+
O2(g)=H2O(g)△H=-483.6KJ/mol,
若1g水蒸气转化成液态水放热2.444kJ,1mol水蒸气变化为液态水放热43.992KJ,②H2O(g)=H2O(l)△H=-43.992KJ/mol,
由盖斯定律①+②得到:H2(g)+
O2(g)=H2O(l)△H=-285.8KJ/mol,
则表示氢气燃烧热的热化学方程式为H2(g)+
O2(g)=H2O(l)△H=-285.8KJ/mol;
故答案为:H2(g)+
O2(g)=H2O(l)△H=-285.8KJ/mol;
(2)丙烯加成聚合生成聚丙烯,反应的化学方程式为: ,为加成聚合反应;
,为加成聚合反应;
故答案为: ,加成聚合反应;
,加成聚合反应;
(3)将N2、H2置于容积为2L的密闭容器中,发生反应,反应进行到4S末,测得N2 2mol、H21.5mol、NH32mol.
N2+3H2=2NH3
起始量(mol)3 4.5 0
变化量(mol) 1 3 2
4s末(mol) 21.5 2
则用氮气浓度的减少来表示该反应的反应速率=
=0.125mol/L?s;
故答案为:0.125mol/L?s;
(4)在500ml密闭容器中,将2mol A和1molB混合加热到500℃,AB的浓度c(A)=4mol/L,c(B)=2mol/L,达到平衡 K=16,设A转化物质的量浓度为x
2A(g)+B (g)?3C(g)
起始量(mol/L) 4 2 0
变化量(mol/L) x 0.5x 1.5x
平衡量(mol/L) 4-x 2-0.5x 1.5x
K=
;
计算得到x=2.284mol/L;
A转化为C的转化率=
×100%=57.1%
故答案为:57.1%;
(5)反应达到平衡后,将气体体积压缩到原来的一半,不考虑平衡移动,物质的浓度变为原来的2倍,题干中A的浓度为原平衡 的2.1倍,说明增大压强平衡逆向进行,aA(g)?cC(g)+dD(g),a<c+d,故答案为:<;
(6)达到平衡时,N的物质的量为2mol,变化6mol,M的物质的量为5mol,变化3mol,反应的方程式为2N?M,故答案为:2N?M.
| 1 |
| 2 |
若1g水蒸气转化成液态水放热2.444kJ,1mol水蒸气变化为液态水放热43.992KJ,②H2O(g)=H2O(l)△H=-43.992KJ/mol,
由盖斯定律①+②得到:H2(g)+
| 1 |
| 2 |
则表示氢气燃烧热的热化学方程式为H2(g)+
| 1 |
| 2 |
故答案为:H2(g)+
| 1 |
| 2 |
(2)丙烯加成聚合生成聚丙烯,反应的化学方程式为:
 ,为加成聚合反应;
,为加成聚合反应;故答案为:
 ,加成聚合反应;
,加成聚合反应;(3)将N2、H2置于容积为2L的密闭容器中,发生反应,反应进行到4S末,测得N2 2mol、H21.5mol、NH32mol.
N2+3H2=2NH3
起始量(mol)3 4.5 0
变化量(mol) 1 3 2
4s末(mol) 21.5 2
则用氮气浓度的减少来表示该反应的反应速率=
| ||
| 4s |
故答案为:0.125mol/L?s;
(4)在500ml密闭容器中,将2mol A和1molB混合加热到500℃,AB的浓度c(A)=4mol/L,c(B)=2mol/L,达到平衡 K=16,设A转化物质的量浓度为x
2A(g)+B (g)?3C(g)
起始量(mol/L) 4 2 0
变化量(mol/L) x 0.5x 1.5x
平衡量(mol/L) 4-x 2-0.5x 1.5x
K=
| (1.5x)3 |
| (4-x)2(2-0.5x) |
计算得到x=2.284mol/L;
A转化为C的转化率=
| 2.284mol/L |
| 4mol/L |
故答案为:57.1%;
(5)反应达到平衡后,将气体体积压缩到原来的一半,不考虑平衡移动,物质的浓度变为原来的2倍,题干中A的浓度为原平衡 的2.1倍,说明增大压强平衡逆向进行,aA(g)?cC(g)+dD(g),a<c+d,故答案为:<;
(6)达到平衡时,N的物质的量为2mol,变化6mol,M的物质的量为5mol,变化3mol,反应的方程式为2N?M,故答案为:2N?M.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目

 2H2(g)+O2(g)。有关该反应的说法正确的是
2H2(g)+O2(g)。有关该反应的说法正确的是