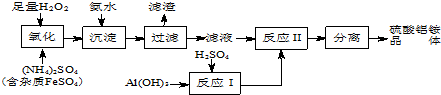
题目内容
14.在下列各溶液中,一定能大量共存的离子组是( )| A. | 常温下水电离的c(OH-)为1×10-12mol/L的溶液中:Fe3+、Na+、SCN-、NO3- | |
| B. | 滴加石蕊后呈蓝色的溶液中:K+、Al3+、Cl-、NO3- | |
| C. | 含有大量HCO3-的澄清透明溶液中:K+、AlO2-、SO4-、Na+ | |
| D. | 常温下c(H+)/c(OH-)=1014的溶液中:K+、Mg2+、Cl-、Br- |
分析 A.常温下水电离的c(OH-)为1×10-12mol/L的溶液,为酸或碱溶液;
B.滴加石蕊后呈蓝色的溶液,显碱性;
C.AlO2-促进HCO3-的电离;
D.常温下c(H+)/c(OH-)=1014的溶液,显酸性.
解答 解:A.常温下水电离的c(OH-)为1×10-12mol/L的溶液,为酸或碱溶液,碱溶液中不能大量存在Fe3+,且Fe3+、SCN-结合生成络离子,不能共存,故A错误;
B.滴加石蕊后呈蓝色的溶液,显碱性,碱性溶液中不能大量存在Al3+,故B错误;
C.AlO2-促进HCO3-的电离,不能大量共存,故C错误;
D.常温下c(H+)/c(OH-)=1014的溶液,显酸性,该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
4.标准状况下,0.4mol HCl气体的体积是( )
| A. | 22.4 L | B. | 11.2 L | C. | 4.48 L | D. | 8.96 L |
5.汽车安全气囊是在发生撞车时、产生二次碰撞前能够自动膨胀保护乘员的装置,碰撞时发生反应:10NaN3+2KNO3═K2O+5Na2O+16N2↑.下列判断正确的是( )
| A. | N2既是氧化剂又是还原剂 | |
| B. | NaN3中N元素被还原 | |
| C. | 每生成16molN2转移30mole- | |
| D. | 还原产物与氧化产物质量之比为1:15 |
9.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| C. | Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O═4 Na++2Cu(OH)2↓+O2↑ |
6.用下列实验装置和方法进行相应实验,能达到实验目的是( )


| A. | 用图甲装置构成锌-铜原电池 | B. | 用图乙装置除去NO2中的NO | ||
| C. | 用图丙装置制备SO2气体 | D. | 用图丁装置制取干燥的氨气 |
3.下列描述与图象相对应的是( )
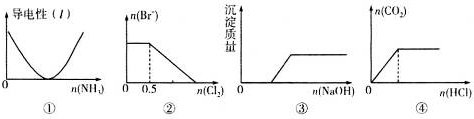

| A. | 图①表示向乙酸溶液中通入氨气至过量的过程中溶液导电性的变化 | |
| B. | 图②表示向1 L l mol•L-1.FeBr2溶液中通入Cl2时Br-物质的量的变化 | |
| C. | 图③表示向Ca(HCO3)2溶液中滴加NaOH溶液时沉淀质量的变化 | |
| D. | 图④表示向一定浓度的Na2CO3溶液中滴加盐酸,生成CO2的物质的量与滴加盐酸物质的量的关系 |
4.下列说法正确的是( )
| A. | 乳酸薄荷醇酯( )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 | |
| B. | 乙醛和丙烯醛(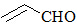 )不是同系物,它们与氢气充分反应后的产物也不是同系物 )不是同系物,它们与氢气充分反应后的产物也不是同系物 | |
| C. | 淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖 | |
| D. | 四联苯(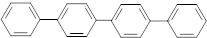 )的一氯代物有4种 )的一氯代物有4种 |