题目内容
【题目】已知(CH3COOH)2(g)2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量随温度(T)的变化曲线如图所示,下列说法正确的是( ) 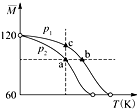
A.该过程的△H<0
B.气体压强:p(a)<p(b)=p(c)
C.平衡常数:K(a)=K(b)<K(c)
D.测定乙酸的相对分子质量要在高压、低温条件
【答案】B
【解析】解:A、温度升高平均摩尔质量减小,气体质量守恒,物质的量增大,说明平衡正反应方向进行,升温平衡向吸热反应方向进行,反应是吸热反应,△H>0,故A错误;B、bc点是压强相同条件下的化学平衡,依据图象分析可知温度不变时,增大压强,气体物质的量减小,气体摩尔质量越大,P1>P2 , 则P(a)<P(b)=P(c),故B正确;
C、a点温度和c点温度相同,b点温度较高,由于反应是吸热反应,因此温度越高平衡常数越大,平衡常数K(b)>K(a)=K(c),故C错误;
D、反应是气体体积增大的吸热反应,测定乙酸的相对分子质量应使平衡正向进行,需要在低压高温条件下进行乙提高乙酸的纯度,故D错误;
故选:B.
A、温度升高平均摩尔质量减小,气体质量不变,物质的量增大,说明平衡正反应方向进行,升温平衡向吸热反应方向进行;
B、bc点是压强相同条件下的化学平衡,依据图象分析可知温度不变时,增大压强,气体物质的量减小,气体摩尔质量越大,P1>P2;
C、平衡常数随温度变化而不随压强变化;
D、反应是气体体积增大的吸热反应,测定乙酸的相对分子质量应使平衡正向进行选择条件.

 口算能手系列答案
口算能手系列答案【题目】试回答下列各题: 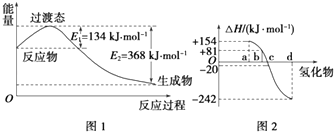
(1)如图1所示是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
(2)化学反应的焓变与反应物和生成物的键能有关.
①已知:H2(g)+Cl2(g)═2HCl(g)△H=﹣185kJmol﹣1
请填空:
共价键 | H﹣H | Cl﹣Cl | H﹣Cl |
键能/(kJmol﹣1) | 436 | 247 |
②图2中表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢在热力学标准状态下,发生分解反应的热化学方程式: .
(3)已知:Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=﹣25kJmol﹣1①
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=﹣47kJmol﹣1②
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+19kJmol﹣1③
请写出CO还原FeO的热化学方程式:
