题目内容
4.(1)在25℃、101kPa下,1g氢气燃烧生成液态水时放热143kJ.则表示氢气燃烧热的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)H2O(l)△H=-286kJ/mol(2)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量.该反应的热化学方程式:C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(l)△H=-1300kJ•mol-1
(3)已知:O2(g)═O2+(g)+e-△H1=+1175.7kJ•mol-1
PtF6(g)+e-═PtF6-(g)△H2=-771.1kJ•mol-1
O2PtF6(s)═O2+(g)+PtF6-(g)△H3=+482.2kJ•mol-1
则反应O2(g)+PtF6(g)═O2PtF6(s)的△H=-77.6 kJ•mol-1.
分析 (1)依据热化学方程式书写方法写出热化学方程式,标注物质聚集状态和对应焓变;
(2)首先根据方程式,推出1mol乙炔燃烧中的电子得失,再据题给条件,转移5mol电子需要乙炔的量,来求算1mol乙炔燃烧放出的热量;
(3)利用盖斯定律解答,从待求反应出发,分析待求反应中的反应物和生成物在已知反应中的位置,通过相互加减可得.
解答 解:(1)25℃、101KPa时,1g氢气燃烧生成液态水时放热143kJ,2g氢气燃烧生成液态水时放热286kJ.则表示H2燃烧热的化学方程式为:H2(g)+$\frac{1}{2}$O2(g) H2O(l)△H=-286 kJ/mol,
故答案为:H2(g)+$\frac{1}{2}$O2(g) H2O(l)△H=-286 kJ/mol;
(2)由题意知:转移电子的物质的量为5mol,又知乙炔燃烧的方程式为2C2H2(g)+5O2(g)═4CO2(g)+2H2O,有2mol乙炔反应时转移20mol电子,
根据方程式计算,设转移5mol电子时有nmol乙炔参加反应,有
2C2H2(g)+5O2(g)═4CO2(g)+2H2O 转移电子
2 20
n 5
n=$\frac{2×5}{20}$=0.5mol,
即,0.5mol乙炔反应放出650kJ的热量,可知1mol乙炔燃烧放出的热量Q=1300KJ,
故答案为:C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(l)△H=-1300 kJ•mol-1;
(5):①O2(g)=O2+(g)+e-△H1=+1175.7kJ•mol-1
②PtF6(g)+e-=PtF6-(g)△H2=-771.1kJ•mol-1
③O2PtF6(S)=O2+(g)+PtF6-(g)△H3=+482.2kJ•mol-1
据盖斯定律,①+②-③得:O2(g)+PtF6(g)=O2PtF6(s)△H=-77.6 kJ•mol-1,
故答案为:-77.6.
点评 本题是书写热化学方程式比较典型的习题,通过氧化还原反应中电子得失来进行△H求算,难度不大.

| A. | 8mol A+4mol B | B. | 2mol A+1mol B | ||
| C. | 6mol C+2mol D+2mol B | D. | 6mol C+2mol D |
| A. | n | B. | $\frac{n}{m}$ | C. | $\frac{12n}{m}$ | D. | n×NA |
| A. | I-、CO32-、SO42- | B. | SO42-、CO32-、I- | C. | CO32-、SO42-、I- | D. | CO32-、I-、SO42- |
(1)已知:2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)△H=-1225kJ.mol-1
| 化学键 | N-H | N-N | N≡N | O-H |
| 键能(kJ.mol-1) | 390 | 190 | 946 | 460 |
(2)800℃时,某密闭容器中存在如下反应:2NO2(g)?2NO(g)+O2(g)△H>0,若开始向容器中加入1mol/L的NO2,反应过程中NO的产率随时间的变化如图曲线I所示.
①反应Ⅱ相对于反应I而言,改变的条件可能是加入催化剂.
②请在图中绘制出在其它条件与反应I相同时,反应在820℃时进行,NO的产率随时间的变化曲线.
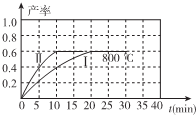
③800℃时,若开始时向容器中同时加入1mol/LNO、0.2mol/LO2、0.55mol/L N02,则v(正)>v(逆)
(3)己知N2H4(g)?2NO2(g)△H=+57.20kJ/mol,t时,将一定量的NO2、N2O4,充人一个容器为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/(mol/L) | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)(mol/L) | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
②前10min内用NO2表示的反应速率为0.04mol/(L.min),20min时改变的条件是增大NO2的浓度;重新达到平衡时,NO2的百分含量b(填选项前字母).
a.增大 b.减小 c.不变 d.无法判断.
①钢较纯铁不易生锈
②冶炼铝和钠都可以用电解法
③KSCN溶液可以检验Fe3+离子
④缺钙会引起骨质疏松,缺铁会引起贫血
⑤青铜、不锈钢、硬铝都是合金.
| A. | ①②③④⑤ | B. | ②③④⑤ | C. | ①③④ | D. | ①②④⑤ |
 .
. .
.