题目内容
用M表示阿伏加德罗常数的数值,下列说法中一定正确的是
- A.1 L l mol?L-1的FeCl3溶液中含有NA个Fe3+
- B.4.8g镁与足量盐酸反应时,转移0.2 NA个电子
- C.钠与水反应生成1.12 L H2,反应中转移的电子数为0.1NA
- D.常温常压下,22g氧气和26g臭氧混合气体所含氧原子总数为3NA
D
分析:A、三价铁离子水解减小;
B、质量换算物质的量,镁全部反应转移电子数根据反应的镁减少;
C、气体摩尔体积的条件应用;
D、质量换算物质的量,氧气和臭氧都是有氧元素组成,结合分子式计算氧原子数;
解答:A、1 L l mol?L-1的FeCl3溶液中含个Fe3+小于NA,故A错误;
B、4.8g镁物质的量为0.2mol,与足量盐酸反应时,转移0.4NA个电子,故B错误;
C、温度和压强未知,钠与水反应生成1.12 L H2物质的量无法计算,故C错误;
D、22g氧气和26g臭氧混合气体中都是氧原子构成的分子,可以直接计算氧原子物质的量为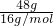 =3mol,故D正确;
=3mol,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要考查盐类水解应用,质量换算物质的量计算微粒数,气体摩尔体积的条件应用.
分析:A、三价铁离子水解减小;
B、质量换算物质的量,镁全部反应转移电子数根据反应的镁减少;
C、气体摩尔体积的条件应用;
D、质量换算物质的量,氧气和臭氧都是有氧元素组成,结合分子式计算氧原子数;
解答:A、1 L l mol?L-1的FeCl3溶液中含个Fe3+小于NA,故A错误;
B、4.8g镁物质的量为0.2mol,与足量盐酸反应时,转移0.4NA个电子,故B错误;
C、温度和压强未知,钠与水反应生成1.12 L H2物质的量无法计算,故C错误;
D、22g氧气和26g臭氧混合气体中都是氧原子构成的分子,可以直接计算氧原子物质的量为
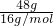 =3mol,故D正确;
=3mol,故D正确;故选D.
点评:本题考查了阿伏伽德罗常数的应用,主要考查盐类水解应用,质量换算物质的量计算微粒数,气体摩尔体积的条件应用.

练习册系列答案
相关题目