题目内容
图甲中电极均为石墨电极,下列叙述中正确的是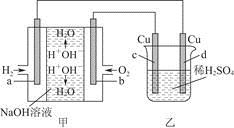
| A.电子沿a→d→c→d路径流动 |
| B.b极的电极反应为O2+4e-+4H+=2H2O |
C.通电初期乙中的总反应为Cu+H2SO4  CuSO4+H2↑ CuSO4+H2↑ |
| D.反应过程中,甲、乙装置中溶液的pH都逐渐减小 |
C
解析 电子可以沿着导线流动,在电解质溶液中是阴阳离子的移动产生电流,即电子沿a→d、c→b路径流动;电池电解质为NaOH,所以b电极的电极反应为O2+4e-+2H2O=4OH-;反应过程中,甲装置中产生水,所以溶液的pH减小,但是乙装置中由于H+被消耗,所以pH增大。

练习册系列答案
相关题目
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以A1作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:电池:Pb(s)+ PbO2(s)+2H2SO4(aq)= 2PbSO4(s)+ 2H2O(l)
电解池:2Al + 3H2O  Al2O3 + 3H2↑,电解过程中,以下判断正确的是( )
Al2O3 + 3H2↑,电解过程中,以下判断正确的是( )
| | 原电池 | 电解池 |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3molPb | 生成2molAl2O3 |
| C | 正极:PbO2+4H++2e-=Pb2++2H2O | 阳极:2Al+3H2O-6e-=Al2O3+6H+ |
| D |  |  |
将两个铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即可产生电流。下列叙述正确的是
①通入CH4的电极为正极 ②正极的电极反应式为O2+2H2O+4e-=4OH- ③通入CH4的电极反应式为CH4+2O2+4e-=CO2+2H2O ④负极的电极反应式为CH4+10OH--8e-=CO32-+7H2O ⑤放电时溶液中的阳离子向负极移动 ⑥放电时溶液中的阴离子向负极移动
| A.①③⑤ | B.②④⑥ | C.④⑤⑥ | D.①②③ |
1 L某溶液中含有的离子如下表:
| 离子 | Cu2+ | Al3+ | NO | Cl- |
| 物质的量浓度(mol/L) | 1 | 1 | a | 1 |
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积的变化及电极产物可能存在的溶解现象),下列说法正确的是( )
A.电解后溶液的pH=0 B.a=3
C.阳极生成1.5 mol Cl2 D.阴极析出的金属是铜与铝
如下图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是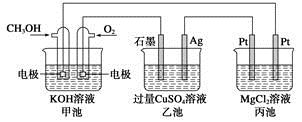
| A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置 |
B.甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=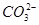 +8H+ +8H+ |
| C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度 |
| D.甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45 g固体 |
一种太阳能电池的工作原理如下图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液,下列说法不正确的是 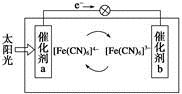
| A.K+移向催化剂b |
| B.催化剂a表面发生的化学反应:[Fe(CN)6]4--e-=[Fe(CN)6]3- |
| C.Fe(CN)在催化剂b表面被氧化 |
| D.电解池溶液中的[Fe(CN)6]4-和[Fe(CN)6]3-浓度基本保持不变 |
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入
| A.0.1 mol CuO | B.0.1 mol CuCO3 |
| C.0.1 mol Cu(OH)2 | D.0.05 mol Cu2(OH)2CO3 |
关于如图所示装置的叙述,正确的是( )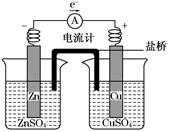
| A.铜是阳极,铜片上有气泡产生 |
| B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 |
| D.铜离子在铜片表面被还原 |
