ĖâÄŋÄÚČÝ
ĄūĖâÄŋĄŋ°ąÆøÄÜÓë―ðĘôŅõŧŊÎï(MxOy) ·īÓĶÉúģÉMĄĒN2šÍH2O,ļųūÝēâķĻģöH2OĩÄÁŋŋÉÍÆģö―ðĘôMĩÄÏāķÔÔŨÓÖĘÁŋĢŽÄģŅÐūŋÐĄŨéÍŽŅ§ÓÃÏÂÁÐŨ°ÖÃ―øÐÐÏāđØĘĩŅéĖ―ūŋĄĢĮëŧØīðÏÂÁÐÎĘĖâ:

(1)°īÆøÁũ·―ÏōĢŽÕýČ·ĩÄŨ°ÖÃ―ÓŋÚËģÐōΊc![]() _________ (ĖîÐōšÅĢŽŨ°ÖÃŋÉÖØļīĘđÓÃ)ĄĢ
_________ (ĖîÐōšÅĢŽŨ°ÖÃŋÉÖØļīĘđÓÃ)ĄĢ
(2)Ũ°ÖÃDÖÐĘĒ·ÅĩÄŌĐÆ·ÃûģÆΊ______,Ũ°ÖÃCĩÄŨũÓÃĘĮ_______.
(3)ČôĘĩŅéÖÐŨžČ·ģÆČĄ―ðĘôŅõŧŊÎïĩÄÖĘÁŋΊzg,ÍęČŦ·īÓĶšóĢŽēâĩÃDÖÐÉúģÉËŪĩÄÖĘÁŋΊwg.ÔōMĩÄÏāķÔÔŨÓÖĘÁŋΊ_____(ÓÚŽxĄĒy zĄĒwĩÄĘ―ŨÓąíĘū)ĄĢ
(4) ÄģÍŽŅ§ŨÐÏļ·ÖÎöÉÏĘöŨ°ÖÚóČÏΊČÔīæÔÚČąÏÝĄĢÄãČÏΊļÃČįšÎļÄ―ø:_________.
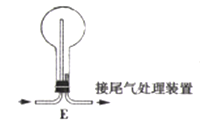
(5) ÄģÍŽŅ§ÓÃŨ°ÖÃAĄĒBĄĒDŌÔž°Ũ°ÖÃE―øÐÐNH;ĩÄīßŧŊŅõŧŊĘĩŅéŅÐūŋĢŽÆäÖÐŨ°ÖÃDĘĒ·ÅĩÄŌĐƷΊNa2O2ĄĢ
ĒŲŨ°ÖÃBÖÐĘĒ·ÅĩÄŌĐƷΊ________.
ĒÚŨ°ÖÃAÖзĒÉú·īÓĶĩÄŧŊŅ§·―ģĖĘ―ÎŠ_____________
ĒÛŅéÖĪÓÐNOÉúģÉĩÄ·īÓĶÏÖÏóΊ_________,EÖзĒÉú·īÓĶĩÄŧŊŅ§·―ģĖĘ―ÎŠ____________
Ąūīð°ļĄŋ f![]() g
g![]() a
a![]() b
b![]() f
f![]() g
g![]() d
d![]() e (fÓëgĢŽaÓëbÎŧÖÃŋÉĩũŧŧ) žîĘŊŧŌŧōĮâŅõŧŊÄÆđĖĖå ÎüĘÕÎī·īÓĶĩÄNH3Ģŧ·ĀÖđŋÕÆøÖÐĩÄËŪÕôÆø―øČëŨ°Öà ( 18zy-16wy)/wx ÔÚÎüĘÕÎēÆøĩÄÅĻÁōËáĮ°žÓ°ēČŦÆŋ·ĀĀýÎü(ŧōÔöžÓ·ĀĀýÎüŨ°ÖÃ) NH4HCO3ŧō(NH4)2CO3 4NH3+5O2
e (fÓëgĢŽaÓëbÎŧÖÃŋÉĩũŧŧ) žîĘŊŧŌŧōĮâŅõŧŊÄÆđĖĖå ÎüĘÕÎī·īÓĶĩÄNH3Ģŧ·ĀÖđŋÕÆøÖÐĩÄËŪÕôÆø―øČëŨ°Öà ( 18zy-16wy)/wx ÔÚÎüĘÕÎēÆøĩÄÅĻÁōËáĮ°žÓ°ēČŦÆŋ·ĀĀýÎü(ŧōÔöžÓ·ĀĀýÎüŨ°ÖÃ) NH4HCO3ŧō(NH4)2CO3 4NH3+5O2![]() 4NO+6H2O Ũ°ÖÃEÖÐģöÏÖšėŨØÉŦÆøĖå 2NO+O2==2NO2
4NO+6H2O Ũ°ÖÃEÖÐģöÏÖšėŨØÉŦÆøĖå 2NO+O2==2NO2
Ąū―âÎöĄŋĢĻ1ĢĐBēúÉúĩÄNH3ūļÉÔïÍĻČëAŨ°ÖÃÖÐĢŽAŨ°ÖÃēúÉúĩÄËŪÓÉDÎüĘÕĢŽŨ°ÖÃCΊÎēÆøÎüĘÕŨ°ÖÃĢŽÕýČ·ĩÄÁŽ―ÓËģÐōΊf![]() g
g![]() a
a![]() b
b![]() f
f![]() g
g![]() d
d![]() eĢŧĢĻ2ĢĐDÖÐÓĶĘĒ·ÅēŧÄÜÓë°ąÆø·īÓĶĩÄļÉÔïžÁĢŽČįžîĘŊŧŌĄĒĮâŅõŧŊÄÆđĖĖåĩČĢŧÓÉÓÚļ÷īÓĶķāÓāĩÄ°ąÆøēŧÄÜÅÅ·Åĩ―īóÆøÖÐĢŽÐčŌŠÓÃÅĻÁōËáÎüĘÕĢŽĮŌÅĻÁōËáÄÜÎüĘÕËŪĢŽ·ĀÖđŋÕÆøÖÐĩÄËŪÕôÆø―øČëŨ°ÖÃÖÐŌýÆðĘĩŅéÎóēîĢŧĢĻ3ĢĐMxOyÖÐŅõÔŨÓĩÄÎïÖĘĩÄÁŋÓëÉúģÉËŪÖÐÆøÔŨÓĩÄÎïÖĘĩÄÁŋÏāĩČĢŽÔōÓÐĢš
eĢŧĢĻ2ĢĐDÖÐÓĶĘĒ·ÅēŧÄÜÓë°ąÆø·īÓĶĩÄļÉÔïžÁĢŽČįžîĘŊŧŌĄĒĮâŅõŧŊÄÆđĖĖåĩČĢŧÓÉÓÚļ÷īÓĶķāÓāĩÄ°ąÆøēŧÄÜÅÅ·Åĩ―īóÆøÖÐĢŽÐčŌŠÓÃÅĻÁōËáÎüĘÕĢŽĮŌÅĻÁōËáÄÜÎüĘÕËŪĢŽ·ĀÖđŋÕÆøÖÐĩÄËŪÕôÆø―øČëŨ°ÖÃÖÐŌýÆðĘĩŅéÎóēîĢŧĢĻ3ĢĐMxOyÖÐŅõÔŨÓĩÄÎïÖĘĩÄÁŋÓëÉúģÉËŪÖÐÆøÔŨÓĩÄÎïÖĘĩÄÁŋÏāĩČĢŽÔōÓÐĢš ![]() =
=![]() ĢŽ―âĩÃM=
ĢŽ―âĩÃM=![]() ĢŧĢĻ4ĢĐÓÉÓÚÅĻÁōËáÄÜŋėËŲÎüĘÕ°ąÆøĢŽĩžÖÂŅđĮŋ―ĩĩÍŌý·ĒĩđÎüĢŽËųŌÔÔÚÎüĘÕÎēÆøĩÄÅĻÁōËáĮ°žÓ°ēČŦÆŋ·ĀĩđÎüŧōÔöžÓ·ĀĩđÎüŨ°ÖÃĢŧĢĻ5ĢĐĒŲļųūÝĖâÄŋĩÄĘĩŅéÄŋĩÄĢŽŨ°ÖÃDÖÐĩÄđýŅõŧŊÄÆÓëËŪŧōķþŅõŧŊĖž·īÓĶēúÉúŅõÆøĢŽÔōBÖÐĘĒ·ÅĩÄŌĐƷΊNH4HCO3ŧō(NH4)2CO3ĢŽĘÜČČ·Ö―âÉúģÉ°ąÆøĄĒķþŅõŧŊĖžĄĒËŪĢŧĒÚAÖзĒÉú°ąÆøīßŧŊŅõŧŊ·īÓĶĢš4NH3+5O2
ĢŧĢĻ4ĢĐÓÉÓÚÅĻÁōËáÄÜŋėËŲÎüĘÕ°ąÆøĢŽĩžÖÂŅđĮŋ―ĩĩÍŌý·ĒĩđÎüĢŽËųŌÔÔÚÎüĘÕÎēÆøĩÄÅĻÁōËáĮ°žÓ°ēČŦÆŋ·ĀĩđÎüŧōÔöžÓ·ĀĩđÎüŨ°ÖÃĢŧĢĻ5ĢĐĒŲļųūÝĖâÄŋĩÄĘĩŅéÄŋĩÄĢŽŨ°ÖÃDÖÐĩÄđýŅõŧŊÄÆÓëËŪŧōķþŅõŧŊĖž·īÓĶēúÉúŅõÆøĢŽÔōBÖÐĘĒ·ÅĩÄŌĐƷΊNH4HCO3ŧō(NH4)2CO3ĢŽĘÜČČ·Ö―âÉúģÉ°ąÆøĄĒķþŅõŧŊĖžĄĒËŪĢŧĒÚAÖзĒÉú°ąÆøīßŧŊŅõŧŊ·īÓĶĢš4NH3+5O2![]() 4NO+6H2OĢŧĒÛNOÓöŨ°ÖÃEÖÐŋÕÆøÉúģÉšėŨØÉŦĩÄNO2ĢŽ·ĒÉú·īÓĶĩÄŧŊŅ§·―ģĖĘ―ÎŠĢš2NO+O2==2NO2ĄĢ
4NO+6H2OĢŧĒÛNOÓöŨ°ÖÃEÖÐŋÕÆøÉúģÉšėŨØÉŦĩÄNO2ĢŽ·ĒÉú·īÓĶĩÄŧŊŅ§·―ģĖĘ―ÎŠĢš2NO+O2==2NO2ĄĢ

 ŧîÁĶŋÎʹ͎ē―Á·Ï°ēáÏĩÁÐīð°ļ
ŧîÁĶŋÎʹ͎ē―Á·Ï°ēáÏĩÁÐīð°ļ Ņ§ŌĩēâÆĀŌŧŋÎŌŧēâÏĩÁÐīð°ļ
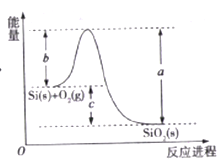
Ņ§ŌĩēâÆĀŌŧŋÎŌŧēâÏĩÁÐīð°ļĄūĖâÄŋĄŋŌŅÖŠ: ĒŲ1molū§ĖåđčÖКŽÓÐ2molSi-SižüĄĢĒÚSi(s)+O2(g)=SiO2(s)ĶĪH,Æä·īÓĶđýģĖÓëÄÜÁŋąäŧŊČįÍžËųĘūĄĢ
ĒÛ
ŧŊŅ§žü | Si-O | O=O | Si-Si |
ķÏŋŠ1molđēžÛžüËųÐčÄÜÁŋ/KJ | 460 | 500 | 176 |
ÏÂÁÐËĩ·ĻÕýČ·ĩÄĘĮ
A. ū§Ėåđčđâ·ü·ĒĩįĘĮ―ŦŧŊŅ§ÄÜŨŠŧŊΊĩįÄÜĩÄ
B. ķþŅõŧŊđčÎČķĻÐÔÐĄÓÚđčĩÄÎČķĻÐÔ
C. ĶĪH=-988 kJ/mol
D. ĶĪH=a-c
ĄūĖâÄŋĄŋÏÂÁÐļũŨéÎïÖĘÖÐĢŽŨéģÉÔŠËØÍęČŦÏāÍŽĩÄĘĮĢĻĄĄĄĄĢĐ
A.ĘŊÄŦÓë―ðļÕĘŊ
B.ËŪŌøÓëŌø
C.ËŪū§ÓëĘŊŧŌĘŊ
D.ĮāÍÓëÍ
ĄūĖâÄŋĄŋÏÂÁÐÓÐđØÎïÖĘĩÄ·ÖĀāÕýČ·ĩÄĘĮ
īŋūŧÎï | ŧėšÏÎï | ĩį―âÖĘ | ËáÐÔŅõŧŊÎï | |
A | ļßÃĖËážØ | ŋÕÆø | īŨËáÄÆ | CO2 |
B | ÏõËá | ŋóČŠËŪ | ÂČŧŊï§ | H2S |
C | ŅÎËá | ËŪŌø | īŋžî | Cl2O |
D | ÂČŧŊÄÆ | ķđ―Ž | Í | N2O5 |
A.AB.BC.CD.D