题目内容
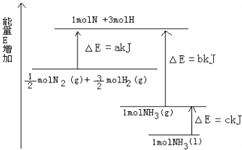
【题目】元素X,Y,Z,M,N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4;M元素原子的最外层电子数与电子层数之比为4:3;N﹣、Z+、X+的半径逐渐减小;化合物XN常温下为气体.据此回答:
①X为(名称),Y为(元素符号),Z原子结构示意图为 .
②N的最高价氧化物的水化物的化学式为 .
③工业上制取单质M的化学方程式为 .
【答案】氢;O; ;HClO4;SiO2+2C
;HClO4;SiO2+2C ![]() Si+2CO↑
Si+2CO↑
【解析】解:元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y原子最外层电子数与核外电子总数之比为3:4,则Y的最外层电子数为6,核外电子数为8符合,即Y为O元素;M元素原子的最外层电子数与电子层数之比为4:3,M为第三周期的Si元素;N﹣、Z+、X+的半径逐渐减小,可知N为Cl、Z为Na、X为H;化合物HCl常温下为气体,①由上述分析可知,X为氢,Y为O,Z的原子结构示意图为  ,所以答案是:氢;O;
,所以答案是:氢;O; 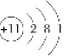 ;②N的最高价氧化物的水化物的化学式为HClO4 , 所以答案是:HClO4;③工业上制取单质M的化学方程式为SiO2+2C
;②N的最高价氧化物的水化物的化学式为HClO4 , 所以答案是:HClO4;③工业上制取单质M的化学方程式为SiO2+2C ![]() Si+2CO↑,所以答案是:SiO2+2C
Si+2CO↑,所以答案是:SiO2+2C ![]() Si+2CO↑.
Si+2CO↑.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目