题目内容
某综合实践小组用废铁屑制FeCl3,用作印刷电路铜板腐蚀剂,并回收铜。活动过程如下:
(1)写出废铁屑与盐酸反应的离子方程式:
①__________________________________;____________________________________。
(2)学生甲对黄色溶液A和绿色溶液C进行定性实验,完成下表:
编号 | 实验内容 | 实验操作 | 预期现象和结论 |
① | 检验黄色溶液A中是否含有Fe2+ |
|
|
② | 检验绿色溶液C中是否含有Fe3+ |
|
|
(3)电解时阴极材料是____________。
(4)采用排液法收集氯气,该液体是____________。
(1)①Fe2O3+6H+![]() 2Fe3++3H2O ②2Fe3++Fe
2Fe3++3H2O ②2Fe3++Fe![]() 3Fe2+
3Fe2+
(2)
编号 | 实验内容 | 实验操作 | 预期现象和结论 |
① | 检验黄色溶液A中是否含有Fe2+ | 取少量黄色溶液A置于小试管中,滴入一滴酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色,则黄色溶液A含有Fe2+ |
② | 检验绿色溶液C中是否含有Fe3+ | 取少量绿色溶液C置于小试管中,滴入一滴KSCN溶液 | 溶液出现血红色,则绿色溶液C含有Fe3+ |
(3)纯铜(粗铜不可)
(4)饱和食盐水
解析:本题考查元素铁和铜的性质,以流程图的形式展示,涉及离子方程式的书写、Fe2+和Fe3+的检验、电解精炼铜以及氯气的收集等知识点。(1)离子方程式的书写考查同学们的基础知识;第(2)问是检验Fe2+和Fe3+的问题,Fe2+可以使酸性高锰酸钾溶液褪色;Fe3+的常用检验方法是用KSCN能变血红色这一特殊现象;(3)电解精炼铜是用纯铜作阴极;(4)Cl2在饱和食盐水中的溶解度小,因而可以用排饱和食盐水的方法来收集氯气。此题只要基础牢固就可顺利得出答案。

练习册系列答案
相关题目
某校综合实践小组用废铁屑制FeCl3,用作印刷电路铜板腐蚀剂,并回收铜.活动过程如下:
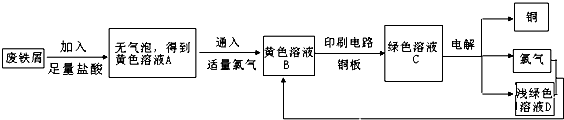
(1)写出废铁屑与盐酸反应的离子方程式: ; .
(2)学生甲对黄色溶液A和绿色溶液C进行定性实验,完成下表:
(3)电解时阴极材料是 .
(4)采用排液法收集氯气,该液体是 .

(1)写出废铁屑与盐酸反应的离子方程式:
(2)学生甲对黄色溶液A和绿色溶液C进行定性实验,完成下表:
| 编号 | 实验内容 | 实验操作 | 预期现象和结论 |
| ① | 检验黄色溶液A中是否含有Fe2+ | ||
| ② | 检验绿色溶液C中是否含有Fe3+ |
(4)采用排液法收集氯气,该液体是




