题目内容
【题目】NH3、NO、N2相互转化关系如图所示(部分产物已略去)。
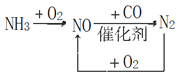
回答下列问题:
(1)N2的电子式是________________________。
(2)写出NH3→NO的化学方程式________________________________。
(3)NO和CO发生反应的化学方程式是_________________________。
(4)NO和O2相遇生成的红棕色气体有毒,可以用NaOH溶液吸收,反应的化学方程式是
![]() ____________。
____________。
【答案】 ![]() 4NH3+5O2
4NH3+5O2 ![]() 4NO +6 H2O 2NO+2CO
4NO +6 H2O 2NO+2CO![]() N2+2CO2 2NaOH+2NO2=== NaNO3+NaNO2+H2O
N2+2CO2 2NaOH+2NO2=== NaNO3+NaNO2+H2O
【解析】试题分析:本题以N2及其化合物的转变为载体,着重考查电子式、基础化学反应原理、氧化还原反应方程式配平等知识。
解析:(1)N2分子中两个N原子通过三对共用电子对形成稳定的分子。正确答案:![]() 。(2)NH3催化氧化原理是4NH3+5O2
。(2)NH3催化氧化原理是4NH3+5O2 ![]() 4NO +6 H2O。正确答案:4NH3+5O2
4NO +6 H2O。正确答案:4NH3+5O2 ![]() 4NO +6 H2O。(3)从关系图可以看出,NO与CO反应可以得到N2,在此过程中NO被还原,所以CO被氧化生成CO2。正确答案:2NO+2CO
4NO +6 H2O。(3)从关系图可以看出,NO与CO反应可以得到N2,在此过程中NO被还原,所以CO被氧化生成CO2。正确答案:2NO+2CO![]() N2+2CO2 。 (4)NO与O2相遇生成的红棕色气体是NO2,已经完成部分说明NO2被还原生成NaNO2,则必有一种物质被氧化,NaOH没有还原性,所以被氧化的物质仍然是NO2,氧化后得到的+5价N的化合物,此题中应当是NaNO3,所以反应物质关系为NaOH+NO2— NaNO3+NaNO2+H2O,再根据得失电子守恒及质量守恒,配平得到2NaOH+2NO2= NaNO3+NaNO2+H2O。正确答案:2NaOH+2NO2= NaNO3+NaNO2+H2O。
N2+2CO2 。 (4)NO与O2相遇生成的红棕色气体是NO2,已经完成部分说明NO2被还原生成NaNO2,则必有一种物质被氧化,NaOH没有还原性,所以被氧化的物质仍然是NO2,氧化后得到的+5价N的化合物,此题中应当是NaNO3,所以反应物质关系为NaOH+NO2— NaNO3+NaNO2+H2O,再根据得失电子守恒及质量守恒,配平得到2NaOH+2NO2= NaNO3+NaNO2+H2O。正确答案:2NaOH+2NO2= NaNO3+NaNO2+H2O。