题目内容
【题目】1,2-二溴乙烷在常温下是无色液体,密度是2.18g/cm3,沸点是131.4℃,熔点是9.79℃,不溶于水,易溶于醇、丙酮等有机溶剂。在实验室可用如图所示装置来制备1,2-二溴乙烷,其中试管c中装有浓溴水。
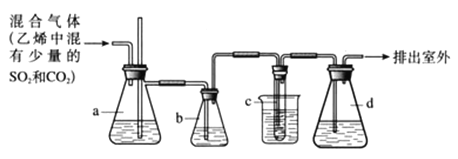
(1)写出制备1,2-二溴乙烷的化学方程式_________________________;
(2)安全瓶a可以防止倒吸,并可以检查实验进行时试管c是否发生堵塞。如果发生堵塞,a中的现象是:____________________________;
(3)容器b中NaOH溶液的作用是____________________________;
(4)将试管c置于冷水中的目的是___________________________;
(5)容器d中NaOH溶液的作用是____________________________。
【答案】 CH2=CH2+Br2→CH2BrCH2Br a中玻璃管内水柱上升,甚至水会溢出 除去乙烯中的CO2和SO2 减少溴的挥发 吸收溴蒸气
【解析】分析:(1)根据溴水与乙烯发生加成反应书写化学方程式;
(2)发生堵塞时a中压强会变大,据此判断;
(3)根据乙烯中含有二氧化硫和二氧化碳判断NaOH溶液的作用是;
(4)根据液溴的物理性质判断;
(5)根据剩余的溴蒸汽需要进行尾气处理解答。
详解:(1)制备1,2-二溴乙烷的化学方程式为CH2=CH2+Br2→CH2BrCH2Br;
(2)如果发生堵塞,a中气压增大,因此可以观察到的实验现象是:a中玻璃管内水柱上升,甚至水会溢出;
(3)乙烯中含有二氧化硫和二氧化碳,会干扰后续实验,则容器b中NaOH溶液的作用是除去乙烯中的CO2和SO2;
(4)由于溴易挥发,所以将试管c置于冷水中的目的是减少溴的挥发;
(5)溴有毒,所以容器d中NaOH溶液的作用是吸收溴蒸气,防止污染空气。

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案
