题目内容
【题目】室温下,对于pH=11的氨水,下列判断正确的是
A. 该氨水的浓度为1.0×10-3mol·L-1
B. 加水稀释,溶液中所有离子的浓度均减小
C. 加水稀释,溶液中c(NH4+)/c(NH3·H2O)变大
D. 与pH=3的盐酸等体积混合,反应后溶液pH=7
【答案】C
【解析】A. 氨水是弱碱,不能完全电离,pH=11的氨水,该氨水的浓度大于1.0×10-3mol·L-1,故A错误;B. NH3·H2O![]() NH4++OH-,加水稀释,溶液中的主要存在离子浓度均会减小,但温度不变,水的离子积常数不变,则c(H+)增大,故B错误;C. NH3·H2O
NH4++OH-,加水稀释,溶液中的主要存在离子浓度均会减小,但温度不变,水的离子积常数不变,则c(H+)增大,故B错误;C. NH3·H2O![]() NH4++OH-,加水稀释,溶液的碱性减弱,c(OH-)减小,但电离常数不变,则溶液中c(NH4+)/c(NH3·H2O)变大,故C正确;D. 氨水是弱碱,不能完全电离,pH=11的氨水,该氨水的浓度大于1.0×10-3mol·L-1,与pH=3的盐酸等体积混合,氨水过量,反应后溶液pH大于7,故D错误;故选C。
NH4++OH-,加水稀释,溶液的碱性减弱,c(OH-)减小,但电离常数不变,则溶液中c(NH4+)/c(NH3·H2O)变大,故C正确;D. 氨水是弱碱,不能完全电离,pH=11的氨水,该氨水的浓度大于1.0×10-3mol·L-1,与pH=3的盐酸等体积混合,氨水过量,反应后溶液pH大于7,故D错误;故选C。

 名校课堂系列答案
名校课堂系列答案【题目】(1)工业上尝试用太阳能分解水制取H2,其过程如下:
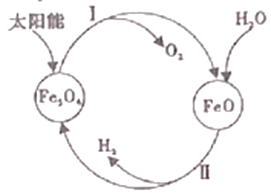
已知:2H2O(l)=2H2(g)+O2(g) △H=+571.6kJ/mol
2Fe3O4(s)![]() 6FeO(s)+O2(g) △H=+313.8kJ/mol
6FeO(s)+O2(g) △H=+313.8kJ/mol
①过程I中,需将O2及时分离出去,目的是_________。
②过程II的热化学方释式是_________。
③整个过程中,Fe3O4的作用是_________。
(2)工业上利用H2合成氢的反应原理为:3H2(g)+N2(g) ![]() 2NH3(g)。现有甲、乙两个容积为1L的密闭容器.在相同条件下,按不同的反应物投入量进行合成氢反应相关数据如下表示:
2NH3(g)。现有甲、乙两个容积为1L的密闭容器.在相同条件下,按不同的反应物投入量进行合成氢反应相关数据如下表示:
容器 | 甲 | 乙 |
反应物投入量 | 2molH2、2molN2 | 4malH2.4molN2 |
平衡时N2的浓度(mol/L) | c1=1.5 | c2 |
NH3的体积分数 | ω1 | ω2 |
混合气体的密度(g/L) | ρ1 | ρ2 |
①下列情况下,反应达到平衡状态的是_____(填序号)
a.3molH-H共价键断裂同时有6molN-H共价键形成
b.3v正(N2)=v逆(H2)
c.混合气体的平均相对分子质量保持不变
②反应的平衡常数K=_______(结果保留3位有效数字).
③分析上表中的数据,有以下关系:c2________3mol/L;ω1________ω2(填“>”、“<”、“=”);若ρ1=ag/L,则ρ2________g/L(用含a的式子表示)
(3)利用氨水吸收工业废气中的SO2,既可解决环境问题,又可制备(NH4)2SO3。可用(NH4)2SO3为原料,以空气氧化法制备(NH4)2SO4,其氧化速率与温度关系如下图:
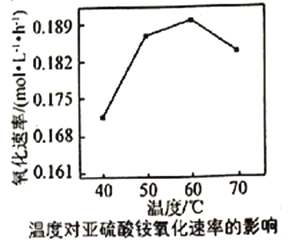
试解释在温度较高时,(NH4)2SO3氧化速率下降的原因是_________。