题目内容
【题目】MgCO3和CaCO3的能量关系如图所示(M=Ca、Mg):
M2+(g)+CO32-(g) ![]() M2+(g)+O2(g)+CO2(g)
M2+(g)+O2(g)+CO2(g)
![]()
![]()
![]()
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
A. ΔH1(MgCO3)>ΔH1(CaCO3)>0
B. ΔH2(MgCO3)=ΔH2(CaCO3)>0
C. ΔH1(CaCO3)-ΔH1(MgCO3)=ΔH3(CaO)-ΔH3(MgO)
D. 对于MgCO3和CaCO3,ΔH1+ΔH2>ΔH3
【答案】C
【解析】
根据盖斯定律,得ΔH=ΔH1+ΔH2+ΔH3,又易知Ca2+半径大于Mg2+半径,所以CaCO3的离子键强度弱于MgCO3,CaO的离子键强度弱于MgO。
A. ΔH1表示断裂CO32-和M2+的离子键所吸收的能量,离子键强度越大,吸收的能量越大,因而ΔH1(MgCO3)>ΔH1(CaCO3)>0,A项正确;
B. ΔH2表示断裂CO32-中共价键形成O2和CO2吸收的能量,与M2+无关,因而ΔH2(MgCO3)=ΔH2(CaCO3)>0,B项正确;
C.由上可知ΔH1(CaCO3)-ΔH1(MgCO3)<0,而ΔH3表示形成MO离子键所放出的能量,ΔH3为负值,CaO的离子键强度弱于MgO,因而ΔH3(CaO)>ΔH3(MgO),ΔH3(CaO)-ΔH3(MgO)>0,C项错误;
D.由上分析可知ΔH1+ΔH2>0,ΔH3<0,故ΔH1+ΔH2>ΔH3,D项正确。
故答案选C。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案【题目】某小组研究FeCl3与Na2S的反应,设计了如下实验:
| 实验a | 实验b | 实验c | |
FeCl3 体积 | 5 mL | 10 mL | 30 mL | |
实验 现象 | 产生黑色浑浊,混合液pH=11.7 | 黑色浑浊度增大,混合液pH=6.8 | 黑色浑浊比实验b明显减少,观察到大量黄色浑浊物,混合液pH=3.7 |
I. 探究黑色沉淀的成分
查阅资料:Fe2S3(黑色)在空气中能够稳定存在,FeS(黑色)在空气中易变质为Fe(OH)3
设计实验:分别取实验a、b、c中沉淀放置于空气中12小时,a中沉淀无明显变化。
b、c中黑色沉淀部分变为红褐色。
(1)① 同学甲认为实验a中黑色沉淀为Fe2S3,实验b、c的黑色沉淀物中既有Fe2S3又有FeS,依据的实验现象是________。
② 同学乙认为实验b的黑色沉淀物中有FeS则一定混有S,理由是_________。
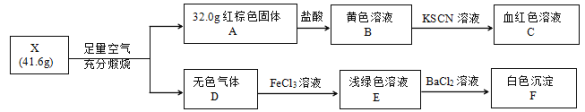
③ 设计实验检验b的黑色沉淀物中混有硫。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
已知:硫在酒精溶液中的溶解度随乙醇质量分数的增大而增大。
实验证明了b中黑色沉淀混有S,试剂a是_____,观察到的现象为_____。
II. 探究实验a中Fe3+与S2-没有发生氧化还原反应的原因
经查阅资料,可能的原因有两种:
原因1:pH影响了Fe3+与S2-的性质,二者不能发生氧化还原反应。
原因2:沉淀反应先于氧化还原反应发生,导致反应物浓度下降,二者不能发生氧化还原反应。
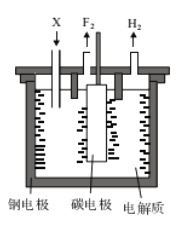
设计实验:电极材料为石墨
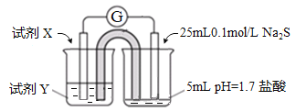
(2)①试剂X和Y分别是__________
②甲认为若右侧溶液变浑浊,说明Fe3+与S2-发生了氧化还原反应。是否合理?说明理由_______。
③乙进一步实验证明该装置中Fe3+与S2-没有发生氧化还原反应,实验操作及现象是_______。
④由此得出的实验结论是__________。
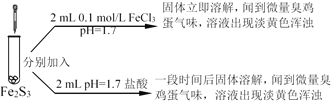
III. 探究实验c随着FeCl3溶液的增加,黑色沉淀溶解的原因
实验1 | 实验2 |
|
|
(3)①用离子方程式解释实验1中的现象_________、_________(写离子方程式)。
②结合化学平衡等反应原理及规律解释实验2中现象相同与不同的原因______。