题目内容
已知溶液中:还原性HSO3->I-,氧化性IO3-> I2 > SO42-。在含3 molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,试回答下列问题:
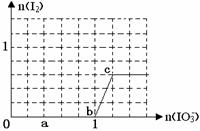
(1)写出a点反应的离子方程式 ;
反应中还原剂是 ;被还原的元素是 。
(2)写出b点到c点反应的离子方程式 。
(3) 当溶液中的I-为0.4 mol时,加入的KIO3为 mol。
当溶液中的I-为0.4 mol时,加入的KIO3为 mol。
(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为
。

(1)写出a点反应的离子方程式 ;
反应中还原剂是 ;被还原的元素是 。
(2)写出b点到c点反应的离子方程式 。
(3)
 当溶液中的I-为0.4 mol时,加入的KIO3为 mol。
当溶液中的I-为0.4 mol时,加入的KIO3为 mol。(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为
。
(1)IO3-+ 3HSO3-→I-+ 3SO42-+3H+(2分)
NaHSO3;(1分)+5价I(1分)。 (2)IO3-+5I-+6H+→3I2+3 H2O(1分)
(3)1.12 mol或0.4 mol 。(2分) (4)2IO3-+ 5HSO3-→I2+ 5SO42-+H2O+3H+(1分)
。(2分) (4)2IO3-+ 5HSO3-→I2+ 5SO42-+H2O+3H+(1分)
NaHSO3;(1分)+5价I(1分)。 (2)IO3-+5I-+6H+→3I2+3 H2O(1分)
(3)1.12 mol或0.4 mol
 。(2分) (4)2IO3-+ 5HSO3-→I2+ 5SO42-+H2O+3H+(1分)
。(2分) (4)2IO3-+ 5HSO3-→I2+ 5SO42-+H2O+3H+(1分)略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 ②Na+结构示意图为
②Na+结构示意图为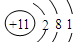
 ⑥
⑥ 与
与 互为同分异构体
互为同分异构体


 物
物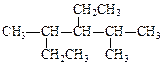 _________________________________
_________________________________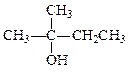 _________________________________
_________________________________ 的结构简式________________________________
的结构简式________________________________ 式为HnXO2n-2,则在其气态氢化物中X元素的化合价为
式为HnXO2n-2,则在其气态氢化物中X元素的化合价为