题目内容
(11分)
“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义。请你回答以下问题:
(1)无机非金属材料。高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:
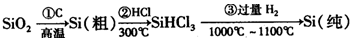
①写出步骤①的化学方程式 。
②步骤②经过冷凝得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点—84.7℃),提纯SiHCl3的主要化学操作的名称是 ;SiHCl3和SiCl4一样遇水可发生剧烈水解,已知SiHCl3水解会生成两种气态产物,请写出其水解的化学方程式 。
③请写出二氧化硅与氢氟酸反应的化学方程式 。
(2)磁性材料。这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施着对它的防护。最常见的铁制品腐蚀就是电化学腐蚀,请出最为普遍的电化学腐蚀的负极反应式 。
(3)激光材料。我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:
, 。
(4)纳米材料。胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直经大约是 ,三氯化铁溶液可以加速伤口止血,请简述原因 。
(5)高分子材料。可以分成无机高分子材料和有机高分子材料。一种新型高效净水剂
[AlFe(OH)nCl6—n]m就属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为 。
一种合成纤维腈纶,又称“人造羊毛”,由丙烯腈(CH2=CH—CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式 。
“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义。请你回答以下问题:
(1)无机非金属材料。高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:
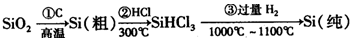
①写出步骤①的化学方程式 。
②步骤②经过冷凝得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点—84.7℃),提纯SiHCl3的主要化学操作的名称是 ;SiHCl3和SiCl4一样遇水可发生剧烈水解,已知SiHCl3水解会生成两种气态产物,请写出其水解的化学方程式 。
③请写出二氧化硅与氢氟酸反应的化学方程式 。
(2)磁性材料。这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施着对它的防护。最常见的铁制品腐蚀就是电化学腐蚀,请出最为普遍的电化学腐蚀的负极反应式 。
(3)激光材料。我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:
, 。
(4)纳米材料。胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直经大约是 ,三氯化铁溶液可以加速伤口止血,请简述原因 。
(5)高分子材料。可以分成无机高分子材料和有机高分子材料。一种新型高效净水剂
[AlFe(OH)nCl6—n]m就属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为 。
一种合成纤维腈纶,又称“人造羊毛”,由丙烯腈(CH2=CH—CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式 。
(1)①SiO2+2C Si+2CO↑
Si+2CO↑
②蒸馏(或分馏)SiHCl3+3H2O==H2SiO3+H2↑+3HCl
③SiO2+4HF==SiF4↑+2H2O
(2)Fe→Fe2++2e-
(3)Al2O3+6H+==2Al3++3H2O Al2O3+2OH-+3H2O==2[Al(OH)4]-
(4)1nm~10nm氯化铁是电解质,使血液胶体聚沉。
(5)+3
 Si+2CO↑
Si+2CO↑②蒸馏(或分馏)SiHCl3+3H2O==H2SiO3+H2↑+3HCl
③SiO2+4HF==SiF4↑+2H2O
(2)Fe→Fe2++2e-
(3)Al2O3+6H+==2Al3++3H2O Al2O3+2OH-+3H2O==2[Al(OH)4]-
(4)1nm~10nm氯化铁是电解质,使血液胶体聚沉。
(5)+3

(1)①写出步骤①的化学方程式:SiO2+2C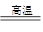 Si+2CO↑
Si+2CO↑
②SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点—84.7℃),由于沸点不同,利用分馏可以提纯,所以,提纯SiHCl3的主要化学操作的名称是分馏。SiHCl3水解的化学方程式:SiHCl3+3H2O=H2SiO3+H2↑+3HCl
③二氧化硅与氢氟酸反应的化学方程式:SiO2+4HF==SiF4↑+2H2O
(2)铁最为普遍的电化学负极反应式:Fe-2e-→Fe2+
(3)Al2O3是两性氧化物,用离子方程式表示为:Al2O3+6H+=2Al3++3H2O
Al2O3+2OH-=2AlO2-+H2O
(4)胶体粒子的直经大约是1nm~10nm之间。三氯化铁溶液可以加速伤口止血,原因:氯化铁是电解质,使血液胶体聚沉。
(5)铁元素的化合价为+3价。
生成该有机高分子材料的化学方程式为: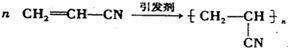
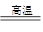 Si+2CO↑
Si+2CO↑②SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点—84.7℃),由于沸点不同,利用分馏可以提纯,所以,提纯SiHCl3的主要化学操作的名称是分馏。SiHCl3水解的化学方程式:SiHCl3+3H2O=H2SiO3+H2↑+3HCl
③二氧化硅与氢氟酸反应的化学方程式:SiO2+4HF==SiF4↑+2H2O
(2)铁最为普遍的电化学负极反应式:Fe-2e-→Fe2+
(3)Al2O3是两性氧化物,用离子方程式表示为:Al2O3+6H+=2Al3++3H2O
Al2O3+2OH-=2AlO2-+H2O
(4)胶体粒子的直经大约是1nm~10nm之间。三氯化铁溶液可以加速伤口止血,原因:氯化铁是电解质,使血液胶体聚沉。
(5)铁元素的化合价为+3价。
生成该有机高分子材料的化学方程式为:
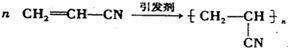

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目