题目内容
【题目】如图为反应2X(g)+Y(s)2Z(g)的反应过程和能量关系图,下列说法正确的是( ) 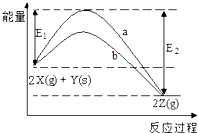
A.曲线a和b表示两个反应过程的反应热不同
B.曲线a一定表示反应是在无催化剂时的反应过程
C.反应达到平衡后,升高温度,平衡常数K值一定减小
D.增大压强,X的转化率一定增大
【答案】C
【解析】解:A、反应的焓变=反应物的总键能﹣生成物的总键能,△H=E1﹣E2 , 所以曲线a和b表示两个反应过程的反应热相同,故A错误;
B、正催化剂能降低反应活化能,而负催化剂能增大反应的活化能,所以曲线a不一定表示反应是在无催化剂时的反应过程,故B错误;
C、依据图象分析,反应物能量高于于生成物,反应是放热反应,升高温度平衡向吸热的方向移动,即逆向反应,平衡常数K值一定减小,故C正确;
D、反应2X(g)+Y(s)2Z(g)前后气体系数之和相等,增大压强平衡不移动,X的转化率不变,故D错误;
故选C.
A、依据反应的焓变=反应物的总键能﹣生成物的总键能,△H=E1﹣E2;
B、依据正催化剂能降低反应活化能,而负催化剂能增大反应的活化能;
C、依据图象分析,反应物能量高于于生成物,反应是放热反应,升高温度平衡向吸热的方向移动,平衡逆向移动,平衡常数K减小;
D、依据前后气体系数之和相等的可逆反应,增大压强平衡不移动.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目