题目内容
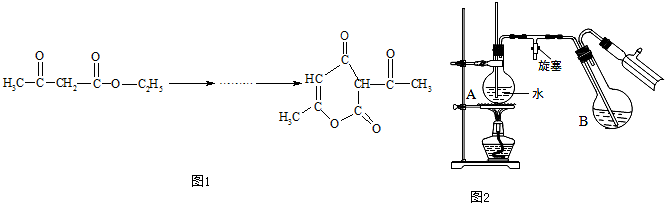
脱氢醋酸是一种难溶于水的低毒、高效广谱抗菌剂,可由乙酰乙酸乙酯经脱醇缩合而成,反应原理为图1:
实验步骤如下:
①在反应器中加入乙酰乙酸乙酯、少量催化剂和数粒沸石,在瓶口安装分馏装置.
②低温加热(不超过85℃)60~70min;然后大火加热蒸出乙醇.
③将反应液趁热倒入烧杯中,冷却到室温,有柠檬黄色晶体析出.
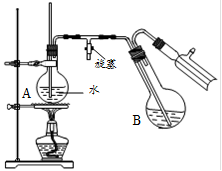
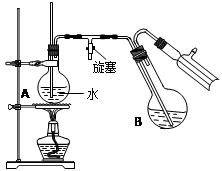
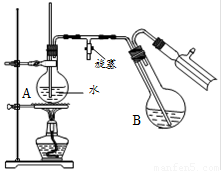
④将柠檬黄色晶体转移至圆底烧瓶B中,加水15mL,滴入1滴硫酸,进行水蒸气蒸馏(如图2所示).从水蒸气蒸馏液中经抽滤可分离出脱氢醋酸,再烘干即得成品.
(1)步骤①中加入沸石的目的是
(2)步骤②中,在60~70min内低温加热的目的是
(3)步骤④中水蒸气蒸馏装置中烧瓶A的作用是
(4)用测得相对分子质量的方法,可以检验所得产物是否纯净,测得相对分子质量通常采用的仪器是
实验步骤如下:

①在反应器中加入乙酰乙酸乙酯、少量催化剂和数粒沸石,在瓶口安装分馏装置.
②低温加热(不超过85℃)60~70min;然后大火加热蒸出乙醇.
③将反应液趁热倒入烧杯中,冷却到室温,有柠檬黄色晶体析出.
④将柠檬黄色晶体转移至圆底烧瓶B中,加水15mL,滴入1滴硫酸,进行水蒸气蒸馏(如图2所示).从水蒸气蒸馏液中经抽滤可分离出脱氢醋酸,再烘干即得成品.
(1)步骤①中加入沸石的目的是
防止暴沸
防止暴沸
.(2)步骤②中,在60~70min内低温加热的目的是
使原料充分反应而不被蒸馏出去
使原料充分反应而不被蒸馏出去
,然后大火加热蒸出乙醇的目的是使平衡正向移动,提高原料的利用率
使平衡正向移动,提高原料的利用率
.(3)步骤④中水蒸气蒸馏装置中烧瓶A的作用是
提供水蒸气
提供水蒸气
,玻璃管的作用是起稳压作用(既能防止装置中压强过大引起事故、又能防止压强过小引起倒吸)
起稳压作用(既能防止装置中压强过大引起事故、又能防止压强过小引起倒吸)
.(4)用测得相对分子质量的方法,可以检验所得产物是否纯净,测得相对分子质量通常采用的仪器是
质谱仪
质谱仪
.分析:(1)加入沸石,可防止暴沸;
(2)步骤②中,在60~70min内低温加热,可防止反应物挥发;反应为可逆反应,从影响平衡移动的角度分析;
(3)进行水蒸气蒸馏,应提供水蒸气,玻璃管可起到平衡烧瓶内大气压的作用;
(4)可用质谱法测定有机物的相关分子质量.
(2)步骤②中,在60~70min内低温加热,可防止反应物挥发;反应为可逆反应,从影响平衡移动的角度分析;
(3)进行水蒸气蒸馏,应提供水蒸气,玻璃管可起到平衡烧瓶内大气压的作用;
(4)可用质谱法测定有机物的相关分子质量.
解答:解:(1)纯液体加热易暴沸,加入沸石,可防止暴沸,故答案为:防止暴沸;
(2)步骤②中,在60~70min内低温加热,可防止反应物挥发,使反应物充分反应;反应为可逆反应,大火加热蒸出乙醇,有利于平衡向正方向移动,提高原料的利用率,
故答案为:使原料充分反应而不被蒸馏出去;使平衡正向移动,提高原料的利用率;
(3)进行水蒸气蒸馏,应提供水蒸气,则水蒸气蒸馏装置中烧瓶A的作用是提供水蒸气,玻璃管可起到平衡烧瓶内大气压的作用,能防止装置中压强过大引起事故、又能防止压强过小引起倒吸,
故答案为:提供水蒸气;起稳压作用(既能防止装置中压强过大引起事故、又能防止压强过小引起倒吸);
(4)可用质谱法测定有机物的相关分子质量,故答案为:质谱仪.
(2)步骤②中,在60~70min内低温加热,可防止反应物挥发,使反应物充分反应;反应为可逆反应,大火加热蒸出乙醇,有利于平衡向正方向移动,提高原料的利用率,
故答案为:使原料充分反应而不被蒸馏出去;使平衡正向移动,提高原料的利用率;
(3)进行水蒸气蒸馏,应提供水蒸气,则水蒸气蒸馏装置中烧瓶A的作用是提供水蒸气,玻璃管可起到平衡烧瓶内大气压的作用,能防止装置中压强过大引起事故、又能防止压强过小引起倒吸,
故答案为:提供水蒸气;起稳压作用(既能防止装置中压强过大引起事故、又能防止压强过小引起倒吸);
(4)可用质谱法测定有机物的相关分子质量,故答案为:质谱仪.
点评:本题以脱氢醋酸的合成为载体综合考查物质的制备方案的设计,侧重于学生实验能力和分析能力的考查,为高考常见题型,题目难度中等,注意把握实验原理和方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目