题目内容
用电子式表示:(1)N2 (2)CO2 (3)硫化钠的形成过程: .
考点:电子式,用电子式表示简单的离子化合物和共价化合物的形成
专题:化学键与晶体结构
分析:氮气分子中,氮原子之间形成3对共用电子对;
二氧化碳为共价化合物,分子中存在两个碳氧双键,氧原子和碳原子最外层都达到8个电子;
硫化钠为离子化合物,钠离子直接用离子符号表示,硫离子需要标出所带电荷和最外层电子.
二氧化碳为共价化合物,分子中存在两个碳氧双键,氧原子和碳原子最外层都达到8个电子;
硫化钠为离子化合物,钠离子直接用离子符号表示,硫离子需要标出所带电荷和最外层电子.
解答:
解:氮原子最外层有5个电子,要达到稳定结构得形成三对共用电子对,氮气的电子式为: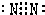 ;
;
碳原子最外层有4个电子,要达到稳定结构要形成四对共用电子对,二氧化碳的电子式为: ,
,
硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物,形成过程为: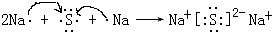 ,
,
故答案为: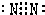 ;
; ;
;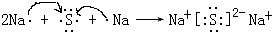 ;
;
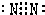 ;
;碳原子最外层有4个电子,要达到稳定结构要形成四对共用电子对,二氧化碳的电子式为:
 ,
,硫化钠是硫离子和钠离子之间通过离子键形成的离子化合物,形成过程为:
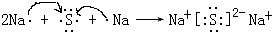 ,
,故答案为:
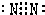 ;
; ;
;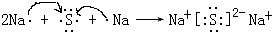 ;
;
点评:本题考查了电子式、用电子式表示离子化合物的形成过程,题目难度中等,注意掌握电子式的概念及表示方法,能够用电子式表示共价化合物和离子化合物的形成过程.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
已知:2NO2(g) N2O4(g)△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g)
N2O4(g)△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g) N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是( )
N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是( )
 N2O4(g)△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g)
N2O4(g)△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g) N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是( )
N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是( )| A、减小NO2的浓度 |
| B、降低温度 |
| C、增加压强 |
| D、升高温度 |
对有机物CH3CH=CH-C≡CH结构的描述正确的是( )
| A、分子中所有碳原子在同一直线上 |
| B、分子中所有氢原子一定在同一平面内 |
| C、分子中在同一平面内的原子最多有6个 |
| D、分子中在同一平面内的原子最多有9个 |
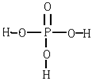 磷酸的结构式如图所示,三分子磷酸可脱去两分子水生成三聚磷酸.含磷洗衣粉中含有三聚磷酸,则该钠盐的化学式及1mol此钠盐中P-O单键的物质的量分别是( )
磷酸的结构式如图所示,三分子磷酸可脱去两分子水生成三聚磷酸.含磷洗衣粉中含有三聚磷酸,则该钠盐的化学式及1mol此钠盐中P-O单键的物质的量分别是( )| A、Na5P3O10 7mol |
| B、Na3H2P3O10 8mol |
| C、Na5P3O10 9mol |
| D、Na2H3P3O10 12mol |
 如图是化学实验常用装置之一,若气体从长管进入,可用来收集的气体是( )
如图是化学实验常用装置之一,若气体从长管进入,可用来收集的气体是( )| A、NO |
| B、NO2 |
| C、H2 |
| D、NH3 |
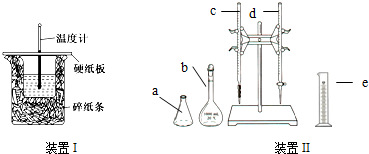
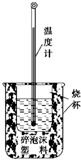 实验室利用如图装置进行中和热的测定.回答下列问题:
实验室利用如图装置进行中和热的测定.回答下列问题: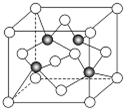 目前大量的照明材料或屏幕都使用了发光二极管(LED).市售LED晶片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.已知镓是铝同族下一周期的元素.砷化镓的晶胞结构如图.试回答:
目前大量的照明材料或屏幕都使用了发光二极管(LED).市售LED晶片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.已知镓是铝同族下一周期的元素.砷化镓的晶胞结构如图.试回答: