题目内容
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图,根据图示判断下列说法正确的是( )

A.H2A在水中的电离方程式是:H2A=H++HA-;HA-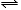 H++A2-
H++A2-
B.当V(NaOH)=20mL时,则有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
D.当V(NaOH)=30mL时,则有:2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2c(OH-)
练习册系列答案
相关题目
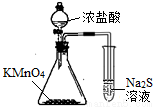
利用下列装置和操作不能达到实验目的的是( )
|
|
|
|
A.从含碘CCl4溶液中提取碘和回收CCl4溶剂 | B.萃取操作过程中的放气 | C.定量测定化学反应速率 | D.比较KMnO4、Cl2、S的氧化性 |


 2NH3 反应,仅改变下列一个条件,就能提高活化分子的浓度从而加快正反应速率的是( )
2NH3 反应,仅改变下列一个条件,就能提高活化分子的浓度从而加快正反应速率的是( )
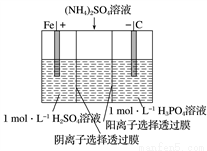
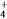 ,模拟装置如图所示。下列说法正确的是( )
,模拟装置如图所示。下列说法正确的是( )