题目内容
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
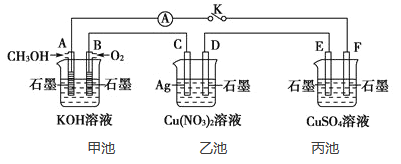
请回答下列问题:
(1)甲池为 (填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为 。
(2)丙池中F电极为 (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为 。
(3)当池中D极质量增重10.8 g时,甲池中B电极理论上消耗O2的体积为 mL(标准状况)。
(4)已知丙池中的溶液为400 mL,合上开关K,一段时间后,丙池中,阳极共收集到气体224 mL(标况下)气体,则此时溶液的pH为 。
【答案】
(1)原电池;CH3OH-6e-+8OH-=CO32-+6H2O;
(2)阴极;2CuSO4+2H2O ![]() 2Cu+O2↑+2H2SO4;
2Cu+O2↑+2H2SO4;
(3)560mL;(4)1;
【解析】
试题分析:(1)甲池能自发进行氧化还原反应为原电池,燃料电池中,燃料失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH3OH+8OH--6e-═CO32-+6H2O,故答案为:原电池;CH3OH+8OH--6e-=CO32-+6H2O;
(2)F连接原电池负极,所以为阴极,阳极上氢氧根离子放电,阴极上铜离子放电,电池反应式为:2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑,故答案为:阴极;2CuSO4+2H2O
2H2SO4+2Cu+O2↑,故答案为:阴极;2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑;
2H2SO4+2Cu+O2↑;
(3)C极上的电极反应为:Ag-e-═Ag+,B电极上的电极反应为:O2+2H2O+4e-═4OH-,当池中C极质量减轻10.8g时,即转移电子是0.1mol,此时甲池中B电极理论上消耗O2的物质的量是0.025mol,体积为0.025mol×22.4L/mol=0.56L=560mL,故答案为:560;
(4)丙池中,阳极上氢氧根离子放电生成氧气4OH- -4e-=2H2O+O2↑,氧气的物质的量为![]() =0.01mol,反应的n(OH-)=0.04mol,因此溶液中c(H+)=0.04mol,n(H+)=0.1mol/L,pH=1,故答案为:1。
=0.01mol,反应的n(OH-)=0.04mol,因此溶液中c(H+)=0.04mol,n(H+)=0.1mol/L,pH=1,故答案为:1。

 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
