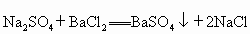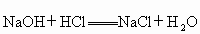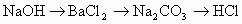题目内容
已知氢氧化镁难溶于水,硫酸钡既不溶于水又不溶于酸,现有主要含有硫酸钠、氯化镁和泥沙的粗食盐,要求从中提出纯净的氯化钠.试说明实验原理及实验方案.
答案:略
解析:
提示:
解析:
|
(1) 实验原理:除去粗盐中的 ①加入过量 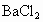 溶液,除去 溶液,除去
②加入过量 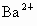
③加入过量 NaOH溶液,除去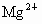
④将③所得混合物过滤,向滤液中加入稍过量的稀盐酸,除去  : :
上述化学试剂的先后顺序,还可以设计为:
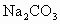 溶液之后是稀盐酸,而稀盐酸必须放在最后. 溶液之后是稀盐酸,而稀盐酸必须放在最后.
(2) 实验方案:(1) 取少量粗食盐放入烧杯中,慢慢加入蒸馏水,并用玻璃棒轻轻搅拌,使氯化钠充分溶解.(2) 用漏斗、滤纸、铁架台(带铁圈)、烧杯等组装过滤装置.将步骤(1)所得混合物进行过滤.若发现滤液浑浊,要再过滤一次,直至溶液澄清.(3) 向(2)所得滤液中加入过量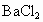 溶液至沉淀不再增加为上,静置沉降. 溶液至沉淀不再增加为上,静置沉降.
(4) 向(3)所得混合物的上层清液中加入过量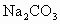 溶液,直至沉淀不再生成为止,静置、沉降. 溶液,直至沉淀不再生成为止,静置、沉降.
(5) 向(4)所得混合物的上层清液中加入过量NaOH溶液,直至沉淀不再生成,静置、沉降.(6) 将(5)所得混合物过滤,向滤液中加入稍过量稀HCl(不再产生气泡或调节溶液pH为7).(7) 把(6)所得溶液倒入蒸发皿中,再把蒸发皿放在高度适宜的铁圈上,用酒精灯加热蒸发皿,并用玻璃棒不断搅动液体,防止因局部温度过高而造成液体飞溅.当蒸发皿中出现较多量固体时,停止加热,用蒸发皿的余热将水分蒸干,即得纯净氯化钠. |
提示:
|
(1) 粗食盐中的泥沙等不溶性杂质,可用过滤的方法除去.(2) 粗食盐中的 等可溶性杂质,应用化学方法使其转化为NaCl.用化学方法除去某物质溶液中的杂质时,为使杂质除得干净,要加入过量的化学试剂,然后再将试剂过量的部分除去.当有多种杂质需要除去并且要使用多种化学试剂时,应考虑不同试剂之间的相互作用,科学设计加入试剂的先后顺序. 等可溶性杂质,应用化学方法使其转化为NaCl.用化学方法除去某物质溶液中的杂质时,为使杂质除得干净,要加入过量的化学试剂,然后再将试剂过量的部分除去.当有多种杂质需要除去并且要使用多种化学试剂时,应考虑不同试剂之间的相互作用,科学设计加入试剂的先后顺序. |

练习册系列答案
相关题目