题目内容
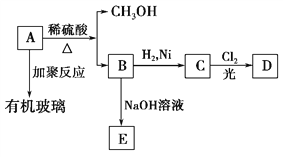
【题目】有机玻璃是一种重要的塑料,有机玻璃的单体A(C5H8O2)不溶于水,并可以发生以下变化:
请回答:
(1)B分子中含有的官能团是________、________。
(2)由B转化为C的反应属于________(选填序号)。
①氧化反应 ②还原反应 ③加成反应 ④取代反应
(3)C的一氯代物D有两种,C的结构简式是________。
(4)由A生成B的化学方程式是___________________________________。
(5)有机玻璃的结构简式是______________________________________。
【答案】 碳碳双键 羧基 ②③ CH3CH(CH3)COOH CH2=C(CH3)COOCH3+H2O![]() CH2=C(CH3)COOH+CH3OH
CH2=C(CH3)COOH+CH3OH 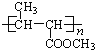
【解析】根据框图中信息A能发生加聚反应,说明其中含有碳碳双键;同时A又能水解生成甲醇,说明A属于酯,B属于羧酸,因此,B中必然含有羧基﹣COOH;又知A水解过程中破坏的只是酯基,而碳碳双键保留了下来,B中应还含有C=C双键,B能与氢气发生加成反应也说明了B含有C=C双键,根据A的分子中有5个碳原子,而它水解又生成了甲醇和B,因此B中有4个碳原子,B转化成C的过程中没有碳原子的变化,即C中也只有4个碳原子,C的一氯代物D有两种,得出C的结构简式为CH3CH(CH3)COOH,故B为CH2=C(CH3)COOH,A为CH2=C(CH3)COOCH3,A加聚反应生成有机玻璃,机玻璃的结构简式是: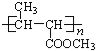 ,
,
(1)B为CH2=C(CH3)COOH,含有碳碳双键、羧基,
(2)CH2=C(CH3)COOH与氢气发生加成反应生成CH3CH(CH3)COOH,该反应也属于还原反应,
(3)由上述分析可知,C为CH3CH(CH3)COOH,
(4)CH2=C(CH3)COOCH3在浓硫酸、加热条件下水解生成甲醇与CH2=C(CH3)COOH,反应方程式为:
CH2=C(CH3)COOCH3+H2O![]() CH2=C(CH3)COOH+CH3OH,
CH2=C(CH3)COOH+CH3OH,
(5)CH2=C(CH3)COOCH3发生加聚反应生成有机玻璃,机玻璃的结构简式是: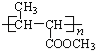 ,
,

【题目】镁的单质及其化合物用途非常广泛。
(1)镁热还原法可制备铷、钛等金属,已知下列物理常数:
Mg | Rb | RbCl | MgCl2 | |
熔点/℃ | 648 | 38.89 | 718 | 714 |
沸点/℃ | 1107 | 688 | 1390 | 1412 |
在750℃时可实现用镁还原RbCl制Rb,该反应能够发生的原因是_________________________________(用文字和化学方程式说明)。
(2)无机抗菌剂Mg2ClO(OH)3·H2O(碱式次氯酸镁)可由MgCl2、NaOH及Cl2反应制得,该反应的化学方程式为______________________________________。
(3)CaC2冶镁的原理为CaC2(s)+MgO(s)![]() CaO(s)+Mg(g)+2C(s) △H,反应达到平衡时Mg的产率随温度的变化如图所示。
CaO(s)+Mg(g)+2C(s) △H,反应达到平衡时Mg的产率随温度的变化如图所示。

①△H__________(填“>"或“<”,下同)0。
②已知A、B中固体总质量相等,则![]() :A__________B。
:A__________B。
(4)Mg(OH)2浆液可脱除烟气中的SO2,其脱硫效率、pH及时间的关系如图所示。

Mg(OH)2浆液脱除SO2的过程中包含的主要反应如下:
Ⅰ.Mg(OH)2+SO2=MgSO3+H2O
Ⅱ.MgSO3+SO2+H2O=Mg(HSO3)2
Ⅲ.Mg(HSO3)2+Mg(OH)2=2MgSO3+2H2O
Ⅳ.2MgSO3+O2=2MgSO4
已知:20℃时,H2SO3的电离平衡常数K1=1.54×10-2、K2=1.02×10-7;25℃时,Ksp[Mg(OH)2]=1.2×10-11,MgSO3,的溶解度为0.646g。
①脱硫过程中使浆液pH减小最显著的反应是__________(填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)。
②约900s之后,脱硫效率明显降低,其原因是________________________。



