题目内容
(4分)已知Na2SO3易被空气氧化变质,欲用氧化还原滴定法来测定实验室里Na2SO3的纯度。取实验室里Na2SO3样品63g,溶于水配成250mL溶液。从其中取出25mL Na2SO3溶液用0.4mol·L-1酸性KMnO4溶液滴定,当溶液刚好变为紫色且半分钟不褪色时,用去40mL酸性KMnO4溶液(已知:5SO32-+2MnO4-+6H+ 5SO42-+2Mn2++3H2O)。则实验室里的Na2SO3的纯度为多少?
(4分)
2KMnO4~5Na2SO3
n(KmnO4)=0.4×0.04=0.016(mol)
n(Na2SO3)=0.04mol(过程2分)
m(Na2SO3)=0.04×10×126=50.4(g)
w(Na2SO3)=50.4÷63×100%=80%(结果2分)
2KMnO4~5Na2SO3
n(KmnO4)=0.4×0.04=0.016(mol)
n(Na2SO3)=0.04mol(过程2分)
m(Na2SO3)=0.04×10×126=50.4(g)
w(Na2SO3)=50.4÷63×100%=80%(结果2分)
试题分析:由题目中的方程式可以得到关系式:5Na2SO3~2KMnO4,可求得Na2SO3的物质的量,然后根据滴定时所取的Na2SO3溶液为所配溶液的
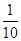 及Na2SO3的摩尔质量可求出原物质中Na2SO3的质量,进一步计算即可求得其纯度。
及Na2SO3的摩尔质量可求出原物质中Na2SO3的质量,进一步计算即可求得其纯度。
练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目