题目内容
有人设计以Pt和Zn为电极材料,埋入人体内作为作为某种心脏病人的心脏起搏器的能源。它依靠跟人体内体液中含有一定浓度的溶解氧、H+和Zn2+进行工作,试写出该电池的两极反应式。
负极:2Zn-4e-= 2Zn2+,正极:O2 + 4H+ + 4e- = 2H2O 。
解析:
金属铂是相对惰性的,金属锌是相对活泼的,所以锌是负极,Zn失电子成为Zn2+,而不是ZnO或Zn(OH)2,因为题目已告诉H+参与作用。正极上O2得电子成为负二价氧,在H+作用下肯定不是O2-、OH-等形式,而只能是产物水,体液内的H+得电子生成H2似乎不可能。故发生以下电极反应:
负极:2Zn-4e-= 2Zn2+,正极:O2 + 4H+ + 4e- = 2H2O 。

练习册系列答案
相关题目
 和
和 进行工作,请写出两极反应的方程式:正极___________,负极___________.
进行工作,请写出两极反应的方程式:正极___________,负极___________.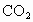 (气态)时放热130 kJ,则乙炔燃烧的热化学方程式为__________________.
(气态)时放热130 kJ,则乙炔燃烧的热化学方程式为__________________.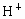 和
和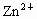 进行工作,请写出两极反应的方程式:正极___________,负极___________.
进行工作,请写出两极反应的方程式:正极___________,负极___________. (气态)时放热130 kJ,则乙炔燃烧的热化学方程式为__________________.
(气态)时放热130 kJ,则乙炔燃烧的热化学方程式为__________________.