��Ŀ����
����Ŀ��C1O2��һ������ɱ��Ч�ʸߡ�������ȾС��ˮ��������ʵ���ҿ�ͨ�����·�Ӧ�Ƶ�C1O2��2KClO3+H2C2O4+H2SO4![]() 2ClO2��+K2SO4+2CO2��+2H2O,����˵������ȷ����
2ClO2��+K2SO4+2CO2��+2H2O,����˵������ȷ����
A. �ڷ�Ӧ��H2C2O4�Ȳ���������Ҳ���ǻ�ԭ��
B. 1 mol KClO3�μӷ�Ӧ���ڱ�״�����ܵõ�22.4 L����
C. 1 mol KClO3�μӷ�Ӧ��2 mol����ת��
D. KClO3�ڷ�Ӧ����������
���𰸡�D
��������
��Ӧ2KClO3+H2C2O4+H2SO4=2ClO2��+K2SO4+2CO2��+2H2O �У�ClԪ�صĻ��ϼ���+5����Ϊ+4�ۣ�CԪ�صĻ��ϼ���+3���ߵ�+4����
A����CԪ�صĻ��ϼ���+3���ߵ�+4�ۣ���H2C2O4�ڷ�Ӧ������ԭ������A����
B����Ӧ��1molKClO3�μӷ�Ӧ������1mol������̼��1molClO2�����ڱ�״�����ܵõ�44.8L���壬��B����
C��ClԪ�صĻ��ϼ���+5����Ϊ+4�ۣ�1molKClO3�μӷ�Ӧת�Ƶĵ���Ϊ1mol����5-4��=1mol����C����
D����Ӧ��ClԪ�صĻ��ϼ���+5����Ϊ+4�ۣ�KClO3�ڷ�Ӧ�еõ����ӣ���KClO3��Ӧ��������������D��ȷ��
��ѡD��

����Ŀ����.��������Դ���²�����ʵ�����ɳ�����չ����Ҫ����ͼ��LiBH4/MgH2��ϵ������ʱ�ʾ��ͼ����Mg(s)+2B(s)==MgB2(s)�Ħ�H=_________kJ��mol-1��
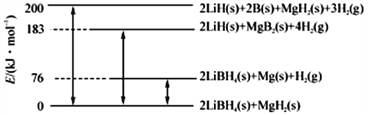
��.��1.0L�����ܱ������з���0.10mol A(g)����һ���¶�ʱ�������·�Ӧ��A(g)==2B(g)+C(g)+D(S) ��H=+85.1kJ��mol-1��
������������ѹǿP����ʼѹǿP0�ı�ֵ�淴Ӧʱ��仯���ݼ��±���
ʱ��t/min | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 |
P/P0 | 1.00 | 1.50 | 1.80 | 2.20 | 2.30 | 2.38 | 2.40 | 2.40 |
�ش��������⣺
��1�����������A��ת���ʵ���______________��
A.�����¶� B.����ϵ��ͨ������A
C. ����D�����ʵ��� D.����ϵ��ͨ��ϡ������
��2������˵���ܱ����÷�Ӧ�ﵽ��ѧƽ��״̬����_______________��
A.A��B��C�����ʵ���֮��Ϊ1��2��1 B.��λʱ��������2n mol B��ͬʱ����n mol C
C.������������ܶȲ��� D.�����������ƽ��Ħ����������
��3���ﵽƽ��״̬ʱA��ת������________�����������λ��Ч���֣���
��4����ͬ�����£����÷�Ӧ������ʼ��������������ͬ�Ļ�ѧƽ�⣬��D��ȡֵ��ΧΪn(D)_______ mol��
��5����ͬ�����£�����������Ϊ��ѹ����������������Ӧ��ijʱ�̣�A��ת����Ϊ75%�����ʱB�����ʵ���Ũ��Ϊ______________mol/L��
����Ŀ��I.������CO2����������ᵼ�µ�������¶�����������̬�����ı䡣
��֪��CO2(g)+CaO(s)![]() CaCO3 (s)
CaCO3 (s)
(1) ij�о�С����ʵ����̽����ͬ�¶ȶ�CaO����CO2Ч�ʵ�Ӱ�졣�������ͬ���ܱ������У�������һ��������ʯ�Һ�����CO2���ڲ�ͬ�¶��£�����������ʼʵ���������䣬��������ƽ��ֱ���t��ʱ�ⶨCO2��Ũ��(mol/L) ��ͼ��
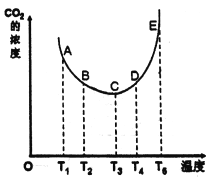
�ٸ÷�Ӧ��__________���������Է����С�
A.�ϸ��¶� B.�ϵ��¶� C.�κ��¶� D.�κ��¶��¾�����
��A��B��C��D��E����У��ﵽ��ѧƽ��״̬�ĵ���_____________��
��2���ں㶨�¶��£�һ������̶�Ϊ1L�������м���20gCaO��һ������CO2���壬��10���Ӵ�ƽ��Ĺ�����CO2Ũ�ȱ仯��ͼ��ʾ��Ϊ���CO2�������ʣ����п��Բ�ȡ�Ĵ�ʩ��__________��
A.��С��Ӧ�������ݻ� B.�����¶�
C.ƽ����ϵ�м�ʱ���������CaCO3 D.ʹ�ú��ʵĴ���
������ƽ��ʱ���¶Ȳ��䣬15����ʱ�����Ѹ��������2L����20����ʱ���´ﵽƽ�⣬������ͼ�в�������仯��CO2Ũ�ȱ仯ʾ��ͼ_______��

��.���ݻ��ɱ���ܱ������з�����Ӧ��mA(g)+nB(g)![]() pC(g),��һ���¶ȺͲ�ͬѹǿ�´ﵽƽ��ʱ���ֱ�õ�A�����ʵ���Ũ�����±�
pC(g),��һ���¶ȺͲ�ͬѹǿ�´ﵽƽ��ʱ���ֱ�õ�A�����ʵ���Ũ�����±�
ѹǿp/Pa | 2��105 | 5��105 | 1��106 |
c(A)mol��L-1 | 0.08 | 0.20 | 0.44 |
��3����ѹǿΪ1��106Paʱ���˷�Ӧ��ƽ�ⳣ������ʽ��_________________________��
��4���縡ѡ���۷��ǹ�ҵ�ϲ��õ�һ����ˮ������������ͼ�Ǹ÷���������ˮ��ʵ��װ��ʾ��ͼ��ʵ������У���ˮ��pHʼ�ձ�����5.0-6.0֮�䡣��ͨ��Դ���������������彫�������ˮ���γɸ�������ȥ����ѡ�������ã����������ij������������ԣ���������������������۾������á�
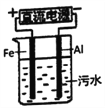
���������ɳ������ܵ缫��ӦΪ��___________________________________��