题目内容
某反应:A(g)+B(g)![]() C(g)在任一时刻的正、逆反应速率可用v正、v逆表示:
C(g)在任一时刻的正、逆反应速率可用v正、v逆表示:
v正=k1c(A)·c(B),v逆=k2c(C),其中k1、k2 在一定温度下均为常数。c(A)、c(B)、c(C)分别表示某时刻三种物质的浓度(mol·L-1)。
⑴上述反应达到平衡时,物质C与A、B的浓度关系可表示为 ;
⑵在300K时,开始反应的A、B浓度均为0.1 mol·L-1,达到平衡时B的转化率为50%,则该温度下k1与k2的关系是 。
答案:
解析:
提示:
解析:
⑴c(C)= (2)k1=20 k2
|
提示:
(1) 达到平衡时v正=v逆 即k1 c(A) c(B)=k2 c(C) 则c(C)= (2) A(g) + B(g)
起始/ mol·L-1 0.1 0.1 平衡/ mol·L-1 0.05 0.05 0.05 由题意300K时:
|

练习册系列答案
相关题目
 pC(g)+qD(s)△H<0如图某反应过程中各物质物质的量n(mol)随时间t的变化曲线图。
pC(g)+qD(s)△H<0如图某反应过程中各物质物质的量n(mol)随时间t的变化曲线图。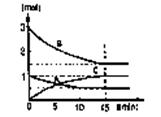
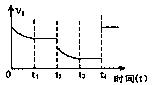
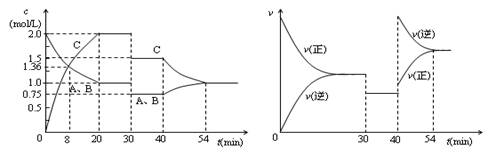
 2C(g)。达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化如下两图所示。
2C(g)。达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化如下两图所示。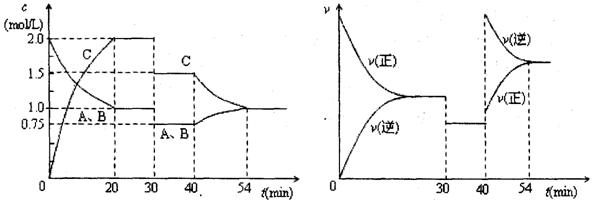
 ·min
·min 2C(g)。达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化如下两图所示。下列说法中正确的是( )
2C(g)。达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化如下两图所示。下列说法中正确的是( )