题目内容
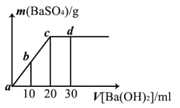
【题目】常温下,向0.1 mol/L的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是
A. 溶液的pH:a<b<c<d
B. 溶液的导电能力:a>b>d>c
C. a、b溶液呈酸性
D. c、d溶液呈碱性
【答案】D
【解析】试题分析:硫酸和氢氧化钡反应方程式为Ba2++2OH-+SO42-+2H+=BaSO4↓+2H2O,根据方程式知,随着反应的进行,溶液中离子浓度逐渐减小直至其完全反应,A.硫酸溶液呈酸性,随着氢氧化钡的加入,溶液中氢离子浓度逐渐减小,pH逐渐增大,所以溶液的pH:a<b<c<d,故A正确;B.溶液导电能力与离子浓度成正比,溶液中离子浓度先减小后增大,所以溶液导电能力先减小后增大,溶液导电能力为a>b>d>c,故B正确;C.硫酸溶液呈酸性,随着氢氧化钡的加入,溶液中氢离子浓度逐渐减小,酸性减弱,a、b点碱不足量,所以溶液呈酸性,故C正确;D.c点酸碱恰好反应生成硫酸钡和水,d点氢氧化钡过量,所以c溶液呈中性、d溶液呈碱性,故D错误。

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案
相关题目