题目内容
在9.5g 某二价金属的氯化物中含有0.20mol Cl-,此氯化物的摩尔质量为________;该金属元素的相对原子质量为________.
95g?mol-1 24
分析:先根据化合物与氯离子间的关系计算氯化物的物质的量,根据M=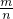 计算其摩尔质量,摩尔质量在数值上等于其相对分子质量,从而确定该金属的原子量.
计算其摩尔质量,摩尔质量在数值上等于其相对分子质量,从而确定该金属的原子量.
解答:某二价金属的氯化物中氯化物的物质的量与氯离子的物质的量之比为1:2,氯离子的物质的量为0.20mol,所以氯化物的物质的量是0.10mol,M=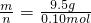 =95g?mol-1;摩尔质量在数值上等于其相对分子质量,所以其相对分子质量为95,其相对分子质量=其相对原子质量+35.5×2=95,所以该金属元素的相对原子质量为24.
=95g?mol-1;摩尔质量在数值上等于其相对分子质量,所以其相对分子质量为95,其相对分子质量=其相对原子质量+35.5×2=95,所以该金属元素的相对原子质量为24.
故答案为:95g?mol-1;24.
点评:本题考查了摩尔质量及物质的量的有关计算,难度不大,明确氯化物与氯离子物质的量的关系是解本题的关键.
分析:先根据化合物与氯离子间的关系计算氯化物的物质的量,根据M=
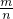 计算其摩尔质量,摩尔质量在数值上等于其相对分子质量,从而确定该金属的原子量.
计算其摩尔质量,摩尔质量在数值上等于其相对分子质量,从而确定该金属的原子量.解答:某二价金属的氯化物中氯化物的物质的量与氯离子的物质的量之比为1:2,氯离子的物质的量为0.20mol,所以氯化物的物质的量是0.10mol,M=
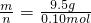 =95g?mol-1;摩尔质量在数值上等于其相对分子质量,所以其相对分子质量为95,其相对分子质量=其相对原子质量+35.5×2=95,所以该金属元素的相对原子质量为24.
=95g?mol-1;摩尔质量在数值上等于其相对分子质量,所以其相对分子质量为95,其相对分子质量=其相对原子质量+35.5×2=95,所以该金属元素的相对原子质量为24.故答案为:95g?mol-1;24.
点评:本题考查了摩尔质量及物质的量的有关计算,难度不大,明确氯化物与氯离子物质的量的关系是解本题的关键.

练习册系列答案
相关题目