题目内容
活性炭可处理大气污染物NO。T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
(1)2 min内,用NO表示该反应的平均速率v(NO)=______mol·L-1·min-1。
(2)该反应的化学方程式是______;T℃时,它的平衡常数K=9/16,则2 min时反应______(填“是”或“不是”)平衡状态;已知升高温度时,K增大,则该反应为______(填“吸热”或“放热”)反应。
(3)为了提高反应速率和NO的转化率,可采取的措施是______。
| | 活性炭/mol | NO/mol | A/mol | B/mol |
| 起始状态 | 2.030 | 0.100 | 0 | 0 |
| 2 min时 | 2.000 | 0.040 | 0.030 | 0.030 |
(1)2 min内,用NO表示该反应的平均速率v(NO)=______mol·L-1·min-1。
(2)该反应的化学方程式是______;T℃时,它的平衡常数K=9/16,则2 min时反应______(填“是”或“不是”)平衡状态;已知升高温度时,K增大,则该反应为______(填“吸热”或“放热”)反应。
(3)为了提高反应速率和NO的转化率,可采取的措施是______。
(1)0.03
(2)C+2NO CO2+N2 是 吸热
CO2+N2 是 吸热
(3)升高温度
(2)C+2NO
 CO2+N2 是 吸热
CO2+N2 是 吸热(3)升高温度
试题分析:(1)v(NO)=?c(NO)/?t=(0.100mol?L?1-0.040mol?L?1)÷2min="0.03" mol·L-1·min-1。
(2)NO和活性炭(无杂质)反应生成气体A和B,由表中数据可知,平衡时C(s)、NO、A、B的物质的量变化分别为0.03mol、0.06mol、0.03mol、0.03mol,故该反应为C+2NO
 CO2+N2;2 min时Q=c(CO2)c(N2)/c2(NO)=0.03×0.03/0.042=9/16=K,所以反应是平衡状态;已知升高温度时,K增大,说明升温平衡向右移动,则该反应为吸热反应。
CO2+N2;2 min时Q=c(CO2)c(N2)/c2(NO)=0.03×0.03/0.042=9/16=K,所以反应是平衡状态;已知升高温度时,K增大,说明升温平衡向右移动,则该反应为吸热反应。(3)升高温度可以提高反应速率,使化学平衡向右移动,提高NO的转化率。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 CH3OH (g) DH1
CH3OH (g) DH1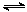 2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大
2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 Y(g) + Z(g) △H<0,反应一段时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示。下列说法中不正确的是
Y(g) + Z(g) △H<0,反应一段时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示。下列说法中不正确的是 2C(气);△H<0 ,经 2 s(秒)后测得 C 的浓度为0.6 mol·L-1 ,现有下列几种说法:
2C(气);△H<0 ,经 2 s(秒)后测得 C 的浓度为0.6 mol·L-1 ,现有下列几种说法: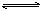 2Z(g);△H<0,在不同温度、不同压强(p1>p2)下,达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为
2Z(g);△H<0,在不同温度、不同压强(p1>p2)下,达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为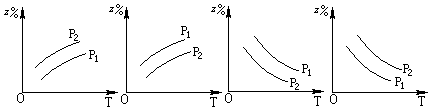
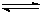 CO(g)+3H2 (g)……I CO(g)+2H2(g)
CO(g)+3H2 (g)……I CO(g)+2H2(g) 

 B(g)+2C(g) ΔH=-50a kJ·mol-1
B(g)+2C(g) ΔH=-50a kJ·mol-1 2Z2在反应过程中的反应速率V与时间(t)的关系曲线,下
2Z2在反应过程中的反应速率V与时间(t)的关系曲线,下