题目内容
【题目】Ⅰ.(1)反应I2+2S2O32-===2I-+S4O62-常用于精盐中碘含量测定。某同学利用该反应探究浓度对反应速率的影响。实验时均加入1 mL淀粉溶液作指示剂,若不经计算,直接通过褪色时间的长短判断浓度与反应速率的关系,下列试剂中应选择____(填序号)。
①1 mL 0.01 mol·L-1的碘水 ②1mL0.001 mol·L-1的碘水
③4 mL 0.01 mol·L-1的Na2S2O3溶液 ④4mL0.001 mol·L-1的Na2S2O3溶液
(2)若某同学选取①③进行实验,测得褪色时间为4s,计算v(S2O32-)=_____。
Ⅱ.一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生反应NO2(g)+SO2(g)![]() SO3(g)+NO(g),下列能说明反应达到平衡状态的是___。
SO3(g)+NO(g),下列能说明反应达到平衡状态的是___。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO2的物质的量之比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
Ⅲ.已知2NO2(g)![]() N2O4(g) ΔH<0。现将NO2和N2O4的混合气体通入恒温恒容为2升的密闭容器中,反应体系中物质浓度随时间的变化关系如图所示。
N2O4(g) ΔH<0。现将NO2和N2O4的混合气体通入恒温恒容为2升的密闭容器中,反应体系中物质浓度随时间的变化关系如图所示。
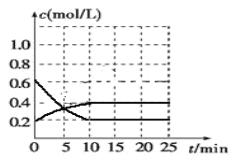
①平衡时NO2的转化率____;②起始压强与平衡时压强之比____。
【答案】②③④ 8.3×10-4 mol·L-1·s-1 b c 66.7% 4:3
【解析】
I(1)用淀粉溶液做指示剂,通过褪色时间判断浓度与反应速率的关系,I2应完全反应,蓝色褪去,采取控制变量法,碘水的浓度不变,改变Na2S2O3溶液浓度;
(2)混合后c(I2)=1mL![]() 0.01mol/L/(1mL+1mL+4mL)=0.01/6mol/L,则v(I2)=
0.01mol/L/(1mL+1mL+4mL)=0.01/6mol/L,则v(I2)=![]() c/
c/![]() t;
t;
II 反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)中,等号两边气体的计量数的和相等;
SO3(g)+NO(g)中,等号两边气体的计量数的和相等;
a.体系压强自始至终保持不变 ,压强不能判断是否达到平衡状态,a错误;
b.反应体系中,NO2(g)有颜色,则平衡时混合气体颜色保持不变,b正确;
c.SO3和NO2的初始物质的量为1:2,反应的物质的量为1:1,则体系中物质的量之比保持不变时,达到平衡状态,c正确;
d.反应过程中,每消耗1 mol SO3的同时必然生成1 molNO2,无法判断是否达到平衡状态,d错误;
Ⅲ.

I(1)用淀粉溶液做指示剂,通过褪色时间判断浓度与反应速率的关系,I2应完全反应,蓝色褪去,采取控制变量法,碘水的浓度不变,改变Na2S2O3溶液浓度,②1mL0.001mol/L的碘水与③4mL0.01mol/L的Na2S2O3溶液、④4mL0.001mol/L的Na2S2O3溶液反应,I2都能完全反应;①1mL0.01mol/L的碘水与④4mL0.001mol/L的Na2S2O3溶液反应,I2不能完全反应,蓝色不能褪去,无法判断,答案为:②③④;
(2)混合后c(I2)=1mL![]() 0.01mol/L/(1mL+1mL+4mL)=0.01/6mol/L,则v(I2)=
0.01mol/L/(1mL+1mL+4mL)=0.01/6mol/L,则v(I2)=![]() c/
c/![]() t=0.01/6mol/L
t=0.01/6mol/L![]() 4s=8.3×10-4 mol/(L·s);
4s=8.3×10-4 mol/(L·s);
II 反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)中,等号两边气体的计量数的和相等;
SO3(g)+NO(g)中,等号两边气体的计量数的和相等;
a.体系压强自始至终保持不变 ,压强不能判断是否达到平衡状态,a错误;
b.反应体系中,NO2(g)有颜色,则平衡时混合气体颜色保持不变,b正确;
c.SO3和NO2的初始物质的量为1:2,反应的物质的量为1:1,则体系中物质的量之比保持不变时,达到平衡状态,c正确;
d.反应过程中,每消耗1 mol SO3的同时必然生成1 molNO2,无法判断是否达到平衡状态,d错误;
答案为bc
Ⅲ.

①平衡时NO2的转化率=0.4/0.6=66.7%;
②起始压强与平衡时压强之比等于物质的量之比,则起始压强与平衡时压强之比=0.8:0.6= 4:3;