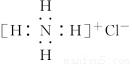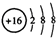题目内容
下列离子方程式中正确的是
A. H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42- = BaSO4↓+2H2O
B. Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++HCO3-+2OH- = CaCO3↓+ CO32-+2H2O
C. Na2CO3溶液中通入少量CO2: CO32-+ CO2+ H2O = 2HCO3-
D. CH3COOH溶液与NaOH溶液反应: H++ OH- = H2O
练习册系列答案
相关题目
A,B,C,D,E,F,G为7种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下,其中:B的离子半径大于E的离子半径;D是由极性键构成的4原子分子;C与F可形成D和G分子。
微粒 | A | B | C | D | E | F | G |
原子核数 | 单核 | 单核 | 多核 | 多核 | 单核 | 多核 | 多核 |
电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
(1)A粒子的结构示意图是_________。
(2)用电子式表示D的形成过程: ________________________
(3)比较B与E相应元素的最高价氧化物对应水化物的碱性强弱,为______>_______(用化学式表示)。
(4)D与G反应的化学方程式是_________________。
(5)C粒子是_________,F粒子是_________(用电子式表示)。

 、
、 和
和 互为同系物
互为同系物