题目内容
在同温同压条件下,一烧瓶充满CO2后质量为124.4g,充满O2后质量为123.2g,充满某未知的气体后质量为122.8g.(1)求这种未知气体的摩尔质量
(2)现测得此气体是由C、H 两种元素组成,且这两种元素的质量比为6:1,试确定此气体的化学式.
【答案】分析:(1)相同容积时,气体的物质的量相同,根据不同气体的质量可得容器的质量,根据n= 可计算A气体的相对分子质量;
可计算A气体的相对分子质量;
(2)根据元素的质量比计算其原子个数之比,再结合其摩尔质量确定化学式.
解答:解:(1)设容器质量为m,某气体摩尔质量为M,利用差量法计算.根据同温同压下,气体质量之差和相对分子质量之差存在正比关系,可得: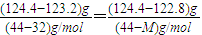 ,解得:M=28g?mol-1,答:该气体的摩尔质量是28g/mol;
,解得:M=28g?mol-1,答:该气体的摩尔质量是28g/mol;
(2)C、H元素的原子个数之比=
 =1:2,设该分子的化学式为CxH2x,其摩尔质量是28g/mol,则12x+2x=28,x=2,所以该分子的化学式为C2H4,答:此气体的化学式为C2H4.
=1:2,设该分子的化学式为CxH2x,其摩尔质量是28g/mol,则12x+2x=28,x=2,所以该分子的化学式为C2H4,答:此气体的化学式为C2H4.
点评:本题考查气体相对分子质量的计算,题目难度不大,注意阿伏加德罗定律定律的灵活应用.
 可计算A气体的相对分子质量;
可计算A气体的相对分子质量;(2)根据元素的质量比计算其原子个数之比,再结合其摩尔质量确定化学式.
解答:解:(1)设容器质量为m,某气体摩尔质量为M,利用差量法计算.根据同温同压下,气体质量之差和相对分子质量之差存在正比关系,可得:
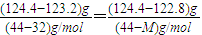 ,解得:M=28g?mol-1,答:该气体的摩尔质量是28g/mol;
,解得:M=28g?mol-1,答:该气体的摩尔质量是28g/mol;(2)C、H元素的原子个数之比=

 =1:2,设该分子的化学式为CxH2x,其摩尔质量是28g/mol,则12x+2x=28,x=2,所以该分子的化学式为C2H4,答:此气体的化学式为C2H4.
=1:2,设该分子的化学式为CxH2x,其摩尔质量是28g/mol,则12x+2x=28,x=2,所以该分子的化学式为C2H4,答:此气体的化学式为C2H4.点评:本题考查气体相对分子质量的计算,题目难度不大,注意阿伏加德罗定律定律的灵活应用.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
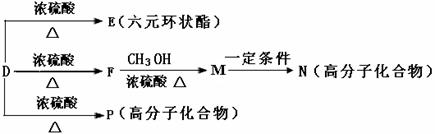
 D→P的化学方程式 反应类型
D→P的化学方程式 反应类型