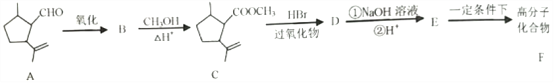
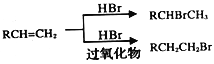
题目内容
【题目】铁氮化合物(![]() )在磁记录材料领域有着广泛的应用前景。某
)在磁记录材料领域有着广泛的应用前景。某![]() 的制备需铁、氮气、丙酮和乙醇参与。
的制备需铁、氮气、丙酮和乙醇参与。
(1)![]() 基态核外电子排布式为_______。
基态核外电子排布式为_______。
(2)丙酮(![]() )分子中碳原子轨道的杂化类型是_______,1mol丙酮分子中含有σ键的数目为______________。
)分子中碳原子轨道的杂化类型是_______,1mol丙酮分子中含有σ键的数目为______________。
(3)C、H、O三种元素的电负性由小到大的顺序为_____。
(4)乙醇的沸点高于丙酮,这是因为_______。
【答案】![]() 或
或![]()
![]() 和
和![]() 9NA
9NA ![]() 乙醇分子间存在氢键
乙醇分子间存在氢键
【解析】
![]()
![]() 的原子序数为26,
的原子序数为26,![]() 基态核外电子数为23,且3d电子为半满稳定结构,可知
基态核外电子数为23,且3d电子为半满稳定结构,可知![]() 基态核外电子排布式为
基态核外电子排布式为![]() 或
或![]() ,故答案为:
,故答案为:![]() 或
或![]() ;
;![]()
![]() 中单键均为
中单键均为![]() 键,双键中含1个
键,双键中含1个![]() 键,甲基上C形成4个
键,甲基上C形成4个![]() 键,
键,![]() 中C形成3个
中C形成3个![]() 键,均没有孤对电子,则羰基上C为
键,均没有孤对电子,则羰基上C为![]() 杂化,甲基上C为
杂化,甲基上C为![]() 杂化,1mol丙酮共有
杂化,1mol丙酮共有![]() 键,数目为
键,数目为![]() 个,故答案为:
个,故答案为:![]() 、
、![]() ;
;![]() ;
;
(3)非金属性越强,电负性越大,则C、H、O三种元素的电负性由小到大的顺序为![]() ,故答案为:
,故答案为:![]() ;
;![]() 乙醇的沸点高于丙酮,这是因为乙醇分子间存在氢键,不仅要破坏分子间作用力,还要破坏氢键,导致沸点高,故答案为:乙醇分子间存在氢键。
乙醇的沸点高于丙酮,这是因为乙醇分子间存在氢键,不仅要破坏分子间作用力,还要破坏氢键,导致沸点高,故答案为:乙醇分子间存在氢键。

练习册系列答案
相关题目