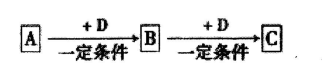
题目内容
硅、铝和铁及其化合物在生产、生活中有广泛应用。请回答下列问题:
(1)Al的原子结构示意图为 ;Al与NaOH溶液反应的离子方程式为
。
(2)30Si原子的中子数为 ,Si的晶体类型为 。
(3)Al3+与Yn—的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是 。
(4)某焊药熔渣36.0g(含Fe2O3、Al2O3、SiO2)加入足量稀盐酸,分离得到11.0g固体,滤液中加入过量NaOH溶液,分离得到21.4g固体。则此熔渣中Al2O3的质量分数为
。
(1)Al的原子结构示意图为 ;Al与NaOH溶液反应的离子方程式为
。
(2)30Si原子的中子数为 ,Si的晶体类型为 。
(3)Al3+与Yn—的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是 。
(4)某焊药熔渣36.0g(含Fe2O3、Al2O3、SiO2)加入足量稀盐酸,分离得到11.0g固体,滤液中加入过量NaOH溶液,分离得到21.4g固体。则此熔渣中Al2O3的质量分数为
。
(1)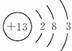 ,2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2↑
,2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2↑
(2) 16 原子晶体 (3) HCl (4)25%
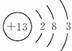 ,2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2↑
,2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2↑(2) 16 原子晶体 (3) HCl (4)25%
试题分析:(1)Al是13号元素,所以Al的原子结构示意图为
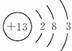 ;Al与NaOH溶液反应的离子方程式为2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2↑。
;Al与NaOH溶液反应的离子方程式为2Al + 2OH-+ 2H2O = 2AlO2-+ 3H2↑。(2)中子数和质子数之和是质量数,30Si原子的中子数为30-14=16。Si的结构与金刚石相似,所以晶体类型为原子晶体。
(3)Al3+与Yn—的电子数相同,所以Y是第二周期的元素。Y所在族各元素的氢化物的水溶液均显酸性,所以是第ⅦA族元素。由于HF分子间存在氢键,所以该族氢化物中沸点最低的是HCl。
(4)二氧化硅与盐酸不反应,所以11.0g固体是二氧化硅。氢氧化铝是两性氢氧化物,能溶解再氢氧化钠溶液中,因此得到的21.4g固体是氢氧化铁,物质的量是0.2mol没声音根据铁原子守恒可知,氧化铁的物质的量是0.1mol,质量是16g,则氧化铝的质量是36.0g-16g-11.0g=9g,因此氧化铝的质量分数是
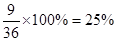 。
。点评:固体是高考中的常见题型,属于基础性试题的考查,难度不大。主要是对学生基础性知识的巩固与检验,同时兼顾对学生能力的培养,有利于培养学生的应试能力,提高学生灵活运用基础知识解决实际问题的能力。

练习册系列答案
相关题目