题目内容
下列离子方程式正确的是
2HCO3-+Ca2++2OH-=2H2O+CaCO3↓+CO32-
| A.在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7 Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B.将少量SO2气体通入NaClO溶液中 SO2+2ClO-+H2O=SO32-+2HClO |
| C.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液 2Fe2+ + 2H+ + H2O2 ="2" Fe3+ + 2H2O |
| D.向NaHCO3溶液中加入过量Ca(OH)2溶液 |
C
A:当两者的物质的量比为2:1时满足题意:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
B:二者应发生氧化还原反应:SO2+ClO-+H2O=SO42-+Cl—+2H+
D:NaHCO3不足,设为1 mol:故HCO3-+Ca2++OH-=H2O+CaCO3↓
B:二者应发生氧化还原反应:SO2+ClO-+H2O=SO42-+Cl—+2H+
D:NaHCO3不足,设为1 mol:故HCO3-+Ca2++OH-=H2O+CaCO3↓

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
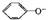 + CO2 + H2O → 2
+ CO2 + H2O → 2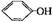 + CO32-
+ CO32- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O H2CO3+2OH-
H2CO3+2OH-