题目内容
化合物E(含两种元素)与NH3反应生成化合物G和H2,G的式量为81.G分子中含硼元素40%、氢元素7.4%.求:
(1)化合物G的化学式.
(2)反应消耗1mol NH3可生成2mol H2,求组成E的元素.
(3)1mol E和2mol NH3恰好完全反应,求化合物E的化学式.
答案:
解析:
解析:
|
(1)由题意E+NH3→G+H2;根据质量守恒定律,G中含氮元素其质量分数为 100%-40%-7.4%=52.6%; G中原子个数比为:B∶N∶H= G的最简式为:BNH2,G的分子量为81,G的化学式为B3N3H6; (2)由上式消耗:1mol NH3时,生成2mol H2,所以E中一定有氢元素,即E为硼、氢化合物; (3)设E的化学式为:BXHY;由反应物和生成物的物质的量关系 则有 3BXHY+6NH3=XB3N3H6+12H2 3X=6; 3Y |

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
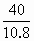 ∶
∶ ∶
∶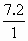 =1∶1∶2
=1∶1∶2 6X=6;解得Y=6;X=2;E的化学式为B2H6
6X=6;解得Y=6;X=2;E的化学式为B2H6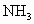 反应,生成化合物G和
反应,生成化合物G和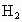 .化合物G的相对分子质量约为8l,G分子中硼元素(B的相对原子质量为10.8和氢元素的质量分数分别是40%和7.4%,由此推断:
.化合物G的相对分子质量约为8l,G分子中硼元素(B的相对原子质量为10.8和氢元素的质量分数分别是40%和7.4%,由此推断: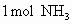 ,可生成
,可生成 ,组成化合E的元素是_________和_________.
,组成化合E的元素是_________和_________.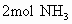 恰好完全反应,化合物E的化学式为___________.
恰好完全反应,化合物E的化学式为___________.