题目内容
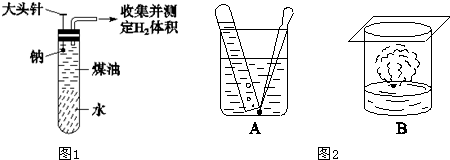
某同学为测定一定质量的钠与水反应产生的H2的体积,设计了图1装置进行实验.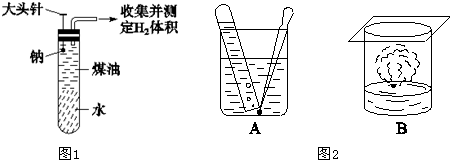
(1)实验开始,欲使钠与水接触反应,应如何操作?______.反应开始后,试管中能观察到的现象是______.
(2)已知有关物质的密度ρ(K):0.86g/cm3,ρ(Na):0.97g/cm3,ρ(煤油):0.8g/cm3.如果将钠换成相同大小的钾进行上述实验,结果钾反应完所用时间比钠反应完所用的时间______(填“长”或“短”),其原因是______.
(3)从实验的安全考虑,比较金属钠、钾与水反应的实验操作图A、图B,请指出图B表示哪种金属与水反应:______.
(4)将一小块钠或钾投入盛饱和硝酸钾的试管里,都不可能观察到的现象是______.
A.熔成小球并在液面上游动
B.有气体生成
C.溶液底部有银白色物质生成
D.溶液变浑浊.
解:(1)要让金属钠和大头针脱离才能和水反应,可以按住橡皮塞,将大头针向上拔出,金属钠和水反应的现象是钠在煤油与水接触的界面之间上下沉浮,
故答案为:按住橡皮塞,将大头针向上拔出;钠在煤油与水接触的界面之间上下沉浮,并不断减小,直到消失,同时有气泡产生.
(2)钾的密度比金属钠的小,钾和水反应产生的氢气可以让金属钾进入煤油中,金属钾和煤油的密度相近,在煤油中滞留时间长,故答案为:长;钾的密度比钠小,与水反应产生少量的气体即可使钾上浮进入煤油中,钾的密度与煤油密度相近,在煤油中滞留时间长;
(3)金属钾和水反应剧烈,为防止生成的碱液伤人,可以在上方罩一个玻璃片,故答案为:钾与水反应;
(4)将金属和水反应,首先会看到金属和水反应的现象:熔、浮、游、响,随着反应的进行,温度升高,硝酸钾的溶解度随文的升高而增大,所以不会出现白色沉淀,故答案为:CD.
分析:(1)可以根据生活实际结合金属钠的物理性质、和水反应的现象来回答即可;
(2)根据金属钾、金属钠以及煤油的密度大小来回答;
(3)根据化学反应的剧烈程度来分析;
(4)钠或钾投入盛饱和硝酸钾的试管里,放热会导致溶液的溶解度发生变化
点评:本题是一道关于金属钠和金属钾与水反应的对比实验知识题目,考查学生分析和解决问题的能力,难度不大.
故答案为:按住橡皮塞,将大头针向上拔出;钠在煤油与水接触的界面之间上下沉浮,并不断减小,直到消失,同时有气泡产生.
(2)钾的密度比金属钠的小,钾和水反应产生的氢气可以让金属钾进入煤油中,金属钾和煤油的密度相近,在煤油中滞留时间长,故答案为:长;钾的密度比钠小,与水反应产生少量的气体即可使钾上浮进入煤油中,钾的密度与煤油密度相近,在煤油中滞留时间长;
(3)金属钾和水反应剧烈,为防止生成的碱液伤人,可以在上方罩一个玻璃片,故答案为:钾与水反应;
(4)将金属和水反应,首先会看到金属和水反应的现象:熔、浮、游、响,随着反应的进行,温度升高,硝酸钾的溶解度随文的升高而增大,所以不会出现白色沉淀,故答案为:CD.
分析:(1)可以根据生活实际结合金属钠的物理性质、和水反应的现象来回答即可;
(2)根据金属钾、金属钠以及煤油的密度大小来回答;
(3)根据化学反应的剧烈程度来分析;
(4)钠或钾投入盛饱和硝酸钾的试管里,放热会导致溶液的溶解度发生变化
点评:本题是一道关于金属钠和金属钾与水反应的对比实验知识题目,考查学生分析和解决问题的能力,难度不大.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案
相关题目
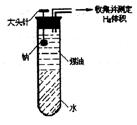 定装置省略)
定装置省略)