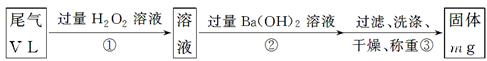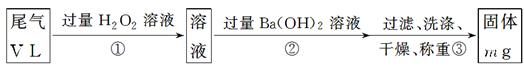题目内容
(14分)硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,分别采用以下方案:
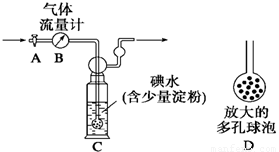
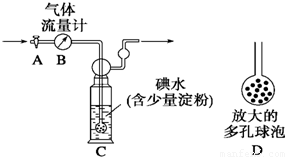
[甲方案]:如图所示,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。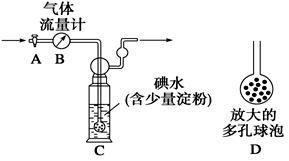
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是_______________________________________。
(2)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量____________(填“偏高”、“偏低”或“无影响”)。
[乙方案]:实验步骤如下面流程图所示: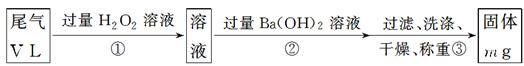
(3)步骤①中过量H2O2的作用是
(4)写出步骤②中反应的化学方程式_______________________________________
(5)步骤②中Ba(OH)2是否足量的判断方法是________________________________
(6)通过的尾气体积为V L(已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为__________________________(用含有V、m的代数式表示)。
(1)增大气体与溶液的接触面积,有利于SO2与碘水充分反应 (2分)
(2) 偏低 (2分)
(3)使SO2完全转化为 SO42- (2分)
(4)H2SO4+Ba(OH)2===B aSO4↓+2H2O (3分)
aSO4↓+2H2O (3分)
(5)静置分层后,往上层清液中继续滴加Ba(OH)2溶液,若无浑浊现象产生,
则Ba(OH)2已足量,反之不足 (2分)
(6) 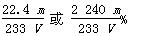 % (3分)
% (3分)
解析

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案