题目内容
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( ) 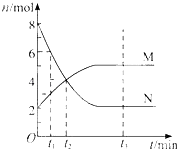
A.反应的化学方程式为:2MN
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
【答案】D
【解析】解:A、由图象可知,反应中M的物质的量逐渐增多,N的物质的量逐渐减少,则在反应中N为反应物,M为生成物,图象中,在相等的时间内消耗的N和M的物质的之比为2:1,所以反应方程式应为:2N ![]() M,故A错误;
M,故A错误;
B、由图可知t2时,反应没有达到平衡,此时反应继续向正方向移动,正反应速率大于逆反应速率,故B错误;
C、由图可知t3时,反应达到平衡,正逆反应速率相等,故C错误;
D、t1时,N的物质的量为6mol.M的物质的量为3mol,故N的浓度是M浓度的2倍,故D正确.
故选D.
A、根据图象判断出反应物和生成物,根据物质的量的变化判断计量数之间的关系;
B、根据某一时间反应中各物质的物质的量是否变化判断反应是否达到平衡;
C、根据平衡移动的方向判断正逆反应速率的关系;
D、根据某一时刻反应物和生成物的物质的量多少判断浓度的关系.

 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案【题目】已知有机物A、C、D、F具有下列性质:
物质 | 性质 |
A | 属于酯类化合物 |
C | 含有4类氢原子 |
D | 只含有一个氧原子,与Na反应放出H2 |
F | 属于烃 |
转化关系如图所示:
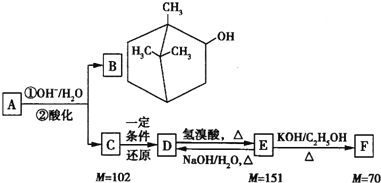
请回答下列问题:
(1)B的分子式为 ____________。
(2)B不能发生的反应是 (_______)(填序号)。
a.氧化反应 b.聚合反应 c.消去反应 d.取代反应 e.与Br2加成反应
(3)写出D→E、E→F的反应:
D→E ____________________________ ;
E→F______________________________。