题目内容
【题目】已知:A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体。
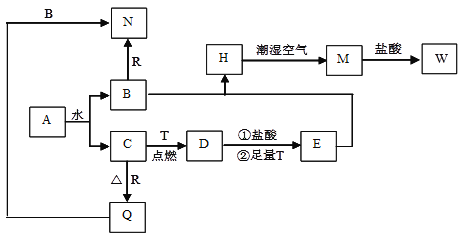
(1)写出下列物质的化学式A_______;D__________;N________。
(2)按要求写下列反应方程式:检验w中阳离子的离子方程式__________________________。
H在潮湿空气中变成M的化学方程式_________________________________。
D与盐酸反应的离子方程式_________________________________。
【答案】 Na2O2 Fe3O4 NaAlO2 Fe3++ 3OH- = Fe(OH)3↓或Fe3++ 3SCN- = Fe(SCN)3 4Fe(OH)2+O2+2H2O====4Fe(OH)3 Fe3O4+8H+====Fe2++2Fe3++ 4H2O
【解析】A为淡黄色固体,A为过氧化钠;D是具有磁性的黑色晶体,D为四氧化三铁;H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体,H为氢氧化亚铁;T、R为两种常见的用途很广的金属单质,可能为铁和铝,根据题意分析可知:T为铁,R为铝;过氧化钠与水反应生成氢氧化钠和氧气,氧气与铁反应生成四氧化三铁,四氧化三铁再与盐酸反应生成氯化亚铁、氯化铁和水,氯化铁溶液再与足量的铁反应生成氯化亚铁;过氧化钠与水反应生成氢氧化钠和金属铝反应生成偏铝酸钠和氢气;最后氯化亚铁溶液与氢氧化钠溶液反应生成氢氧化亚铁白色沉淀,在空气中氧化为氢氧化铁,最后和盐酸反应生成氯化铁溶液。
(1)根据以上分析可知:A为Na2O2、D为Fe3O4、N为NaAlO2;正确答案:Na2O2、Fe3O4、NaAlO2。
(2)w中阳离子为Fe3+,其检验方法为:滴加氢氧化钠溶液,生成红褐色沉淀,Fe3++ 3OH- = Fe(OH)3↓;或滴加硫氢化钾溶液,溶液变为血红色,Fe3++ 3SCN- = Fe(SCN)3;正确答案:Fe3++ 3OH- = Fe(OH)3↓或Fe3++ 3SCN- = Fe(SCN)3。氢氧化亚铁白色沉淀,在空气中氧化为氢氧化铁,化学方程式为4Fe(OH)2+O2+2H2O====4Fe(OH)3 ;正确答案:4Fe(OH)2+ O2+2H2O====4Fe(OH)3。四氧化三铁与盐酸反应生成氯化亚铁、氯化铁和水,反应的离子方程式:Fe3O4+8H+==Fe2++2Fe3++ 4H2O;正确答案:Fe3O4+8H+==Fe2++2Fe3++ 4H2O。