题目内容
【题目】医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含量.回答下列问题:
(1)配平以下离子方程式,并填上所需的微粒.
H++MnO4﹣+H2C2O4→CO2↑+Mn2++
(2)标出电子转移的方向和数目
(3)该反应中的还原剂是;氧化产物是 .
(4)反应转移了0.4mol电子,则消耗KMnO4的物质的量为mol.
【答案】
(1)6,2,5,10,2,8H2O
(2)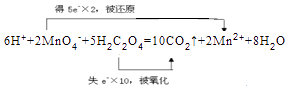
(3)H2C2O4,CO2
(4)0.08
【解析】解:(1)根据元素守恒知,生成物中还含有水,该反应中Mn元素化合价由+7价变为+2价、C元素化合价由+3价变为+4价,其转移电子总数为10,所以MnO4﹣、H2C2O4的计量数分别是2、5,再结合原子守恒配平方程式为6H++2MnO4﹣+5H2C2O4=10CO2↑+2Mn2++8H2O,
所以答案是:6;2;5;10;2;8H2O;(2)反应中MnO4﹣→Mn2+,Mn元素由+7价→+2价,一个MnO4﹣得5个电子;H2C2O4→CO2,C元素由+3价→+4价,一个H2C2O4失去2个电子,化合价升高值=化合价降低值=转移电子数=10,则反应6H++2MnO4﹣+5H2C2O4=10CO2↑+2Mn2++8H2O,电子转移情况如下: 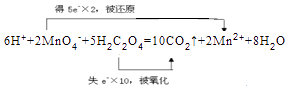 ,
,
所以答案是:2;5;16H+;2;10;8H2O; 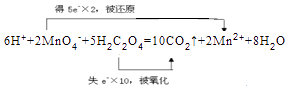 ;(3)失电子化合价升高的反应物H2C2O4是还原剂,发生氧化反应,对应的产物为氧化产物,则氧化产物是CO2,
;(3)失电子化合价升高的反应物H2C2O4是还原剂,发生氧化反应,对应的产物为氧化产物,则氧化产物是CO2,
所以答案是:H2C2O4;CO2; (4)根据MnO4﹣﹣﹣﹣5e﹣得,反应转移了0.4mol电子,则消耗KMnO4的物质的量= ![]() =0.08mol,
=0.08mol,
所以答案是:0.08.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

