题目内容
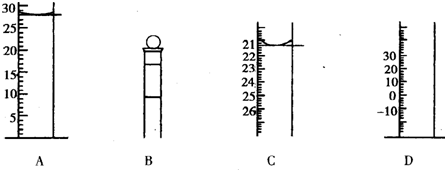
下图四种化学实验操作,其中正确的是( )
分析:A.NaOH应放在小烧杯中称量;
B.钠燃烧放出热量,可在坩埚中进行;
C.分液时,下端紧靠烧杯内壁;
D.加水应利用玻璃棒引流,且不能在容量瓶中直接配制.
B.钠燃烧放出热量,可在坩埚中进行;
C.分液时,下端紧靠烧杯内壁;
D.加水应利用玻璃棒引流,且不能在容量瓶中直接配制.
解答:解:A.NaOH易吸水,具有腐蚀性,则NaOH应放在小烧杯中称量,不放在纸片上,故A错误;
B.钠燃烧放出热量,可在坩埚中进行,图中装置合理,故B正确;
C.分液时,下端紧靠烧杯内壁,分离时下层液体从下口放出,故C错误;
D.加水应利用玻璃棒引流,且不能在容量瓶中直接配制,应在烧杯中溶解冷却吼吼转移到容量瓶中,故D错误;
故选B.
B.钠燃烧放出热量,可在坩埚中进行,图中装置合理,故B正确;
C.分液时,下端紧靠烧杯内壁,分离时下层液体从下口放出,故C错误;
D.加水应利用玻璃棒引流,且不能在容量瓶中直接配制,应在烧杯中溶解冷却吼吼转移到容量瓶中,故D错误;
故选B.
点评:本题考查化学实验方案的评价,涉及称量、溶解、溶液配制、分液等实验操作,侧重实验基本操作和实验注意点的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目