题目内容
在pH相同,体积相等的盐酸A和醋酸溶液B中,分别加入等质量的锌,若反应停止后,有一份溶液中锌有剩余,则正确的判断是( )
①反应所需时间B>A;②开始时反应速度A>B
③参加反应的锌的质量B>A;④整个反应阶段平均速度B>A
⑤盐酸中锌有剩余;⑥醋酸溶液中锌有剩余
⑦盐酸中放氢气多;⑧醋酸溶液中放氢气多.
①反应所需时间B>A;②开始时反应速度A>B
③参加反应的锌的质量B>A;④整个反应阶段平均速度B>A
⑤盐酸中锌有剩余;⑥醋酸溶液中锌有剩余
⑦盐酸中放氢气多;⑧醋酸溶液中放氢气多.
分析:醋酸是弱电解质,醋酸溶液中存在电离平衡,氯化氢是强电解质,所以等pH的醋酸和盐酸,醋酸的物质的量浓度大于盐酸,等体积等pH的盐酸和醋酸,醋酸的物质的量大于盐酸,加入等质量的锌,若反应停止后,若有一份溶液中锌有剩余,则有锌剩余的酸是盐酸.
解答:解:醋酸是弱电解质,醋酸溶液中存在电离平衡,氯化氢是强电解质,所以等pH的醋酸和盐酸,醋酸的物质的量浓度大于盐酸,等体积等pH的盐酸和醋酸,醋酸的物质的量大于盐酸,加入等质量的锌,若反应停止后,若有一份溶液中锌有剩余,则有锌剩余的酸是盐酸,
①醋酸是弱电解质,溶液中存在电离平衡,反应过程中,醋酸溶液中氢离子浓度始终大于盐酸,则反应速率醋酸始终大于盐酸,所以反应所需时间B<A,故错误;
②开始时氢离子浓度相等,所以反应速度A=B,故错误;
③等体积等pH的盐酸和醋酸,醋酸的物质的量大于盐酸,所以参加反应的锌的质量B>A,故正确;
④反应过程中,醋酸溶液中氢离子浓度始终大于盐酸,则反应速率醋酸始终大于盐酸,所以整个反应阶段平均速度B>A,故正确;
⑤盐酸的物质的量小于醋酸,所以盐酸中锌有剩余,故正确;
⑥盐酸的物质的量小于醋酸,所以盐酸中锌有剩余,醋酸溶液中锌没有剩余,故错误;
⑦盐酸的物质的量小于醋酸,所以醋酸中放氢气多,故错误;
⑧盐酸的物质的量小于醋酸,所以醋酸中放氢气多,故正确;
故选A.
①醋酸是弱电解质,溶液中存在电离平衡,反应过程中,醋酸溶液中氢离子浓度始终大于盐酸,则反应速率醋酸始终大于盐酸,所以反应所需时间B<A,故错误;
②开始时氢离子浓度相等,所以反应速度A=B,故错误;
③等体积等pH的盐酸和醋酸,醋酸的物质的量大于盐酸,所以参加反应的锌的质量B>A,故正确;
④反应过程中,醋酸溶液中氢离子浓度始终大于盐酸,则反应速率醋酸始终大于盐酸,所以整个反应阶段平均速度B>A,故正确;
⑤盐酸的物质的量小于醋酸,所以盐酸中锌有剩余,故正确;
⑥盐酸的物质的量小于醋酸,所以盐酸中锌有剩余,醋酸溶液中锌没有剩余,故错误;
⑦盐酸的物质的量小于醋酸,所以醋酸中放氢气多,故错误;
⑧盐酸的物质的量小于醋酸,所以醋酸中放氢气多,故正确;
故选A.
点评:本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,注意反应速率与氢离子浓度成正比,与酸的强弱无关,为易错点.

练习册系列答案
相关题目
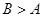 ;②开始时反应速度
;②开始时反应速度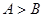
 ;②开始时反应速度
;②开始时反应速度